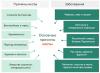
Чистата естествена сяра е жълто кристално твърдо вещество. В природата сярата се среща в естествена форма, образувайки големи находища. Колекционният материал представлява добре оформени и ярко оцветени серни кристали с диамантен и матов блясък с размери 1,5-15 см или повече, както и четки и друзи от такива кристали.
От древни времена сярата се използва широко в експериментите на алхимиците и в медицината. При изгаряне издава силна характерна миризма. Ароматът и цветът му карат хората да използват сярата в магията от векове. Често се изгаря, за да се предпазят от „демони“ и „дяволи“. Това се дължи на идеята, че положителните сили ще бъдат привлечени от приятните аромати, докато отрицателните сили ще мразят неприятните миризми и ще бягат от тях. По-късно сярата била изгаряна, за да защити животните и да спре „омагьосването“ или магическото поробване.
Сярата е постоянен компонент на растенията, тя се съдържа в тях под формата на различни неорганични и органични съединения. Неорганичната сяра се намира под формата на соли на сярна киселина. Известни са бактериите, които го концентрират. Някои от микроорганизмите образуват специфични серни съединения като отпадъчни продукти; например гъбите от рода Penicillinum синтезират съдържащия сяра антибиотик пеницилин.
Сярата, подобно на азота, е част от протеините, поради което протеиновият метаболизъм е както азотен, така и серен. В тъканите сярата се намира под формата на сложни органични съединения - сулфати, или в комбинация с въглехидрати, или под формата на сулфатиди в комбинация с фосфатиди в така наречените липоиди, които изграждат медулата.
Сярата се съдържа в инсулина и някои изследователи приписват хипогликемичния ефект на инсулина на съдържащата се в него сяра.
Сярата се съдържа в антиневралгичния витамин В-тиамин, който отличава този витамин от останалите. В протеините сярата се съдържа в аминокиселини: цистеин, цистин, които участват в редокс реакциите на тялото. Цистеинът е част от глутатиона, протеиново вещество, което е богато на червените кръвни клетки, черния дроб, надбъбречните жлези и особено ембрионалната тъкан, в която протичат много интензивни окислителни процеси.
Участвайки в редокс процесите, сярата играе същата роля в тъканното дишане като хемоглобина и оксихемоглобина в газообмена в белите дробове.

Елементарната сяра няма изразен токсичен ефект, но всички нейни съединения са токсични. Приета през устата, 3 - 5 g елементарна сяра действа слабително поради образуването на сероводород в червата, стимулиращ перисталтиката. Но при ежедневен прием на малки дози сяра от 1,0-2,5-10 mg за 1-2 седмици се появяват главоболие, световъртеж, умора, изпотяване, ускорен пулс, запек, болки в корема, промени в метаболизма и др.
Сярата и нейните неорганични съединения се използват в медицината от древни времена за кожни заболявания, ставни заболявания, отравяне с тежки метали и като слабително средство.
Фумигацията със сяра спира хремата. Налага се на смачканото ухо с оцет и мед.
Лечебните свойства на сярата се използват много широко в балнеологията. Действието на серните води се дължи на съдържащия се в тях сероводород. Абсорбиран през кожата и белите дробове, сероводородът причинява зачервяване на кожата от разширяването на най-малките кръвоносни съдове в кожата, забавяне на пулса с 10-15 удара и намаляване на систолното и диастоличното налягане с 5-10 mm . Лечението със сярни води се прилага при различни видове заболявания: хронична артропатия с ревматична и подагрозна етиология, заболявания на сърдечния мускул като кардиосклероза, остеомиелит с повтарящи се фистули, хронични женски болести, хронични кожни заболявания, отравяне с живак и олово по време на работа.
Противопоказания за лечение със сярни води са остри и подостри заболявания на сърцето, ставите, женските органи, хипертония със симптоми на нефросклероза, костна анкилоза, фурункулоза и всички пиодермични заболявания.
Понастоящем се използват следните неорганични серни съединения:
Natrium hyposulfurosum, натриев тиосулфат (хипосулфат) се използва (според метода на Демянович) като външно средство за лечение на краста и някои гъбични кожни заболявания.
Sulphur depuratum, пречистена сяра (Flos sulfurise, сярен цвят), се използва като слабително средство при запек (0,5-1,0 g на доза) и за лечение на ентеробиоза (инфекция с острици). Включен в комплексен прах от женско биле (Pulvis Glycyrrhisae compositae). През 1926 г. датският психиатър К. Шрьодер предлага лечение с интрамускулни инжекции от 1% пречистена сяра за заболявания като невролуес, табес, парализа и шизофрения.

Външно се използва в мехлем на Wilkinson и проста сяра.
Calcium sulfuricum, калциев сулфат, освобождава вода при нагряване и се превръща в изгорял гипс, използван в хирургията за превръзки.
През последните 20 години медицината започна широко да използва препарати от органична сяра. През 1935 г. немският учен Domagk предлага лекарството Prontosil, съдържащо сулфогрупа 802. Това лекарство се оказва ефективно в борбата с микробите. Фармацевтичната индустрия е създала голям брой сулфонамидни лекарства. Най-простата химическа структура е бял стрептоцид. Всички други сулфонамидни лекарства са производни на белия стрептоцид. Това са сулфадин, сулфазол, норсулфазол, сулфазин, сулфадимезин, уросулфан, дисулфан, сулгин, фталазол, сулфозин и др. Всички тези лекарства са високоактивни средства в борбата срещу тежки заболявания, причинени от коки и бацили, върху които те
произвеждат бактериостатичен ефект, но съдържанието в тях, освен бензен, амидо и сулфо групи може да доведе до странични ефекти.
В хомеопатията се използва както елементарната сяра, така и нейните различни съединения, но начело на всички серни съединения стои елементарната сяра – Sulphur. Сярата е многократно изпитана от Ханеман, в нея той вижда основното средство срещу основното страдание на човечеството – “псора”. С този термин Ханеман обединява всички кожни заболявания, изразяващи се със сърбеж, обриви, брадавици и други кожни изменения. Опитът показва, че сярата е лекарство, което рядко може да се отмени при лечението на тежки остри заболявания и никога при лечение на хронични.
Сярата е най-силният активатор на различни нарушения на метаболизма на сярата (протеините) и наистина е лекарство от първостепенно значение. Селективността на сярата към кожата отдавна я е превърнала в основно средство за лечение на кожни заболявания. Сярата се използва и при заболявания на централната нервна система, което е лесно обяснимо: кожата и нервната система са свързани от общ произход.
Но употребата на сяра, дори и в хомеопатични дози, изисква голямо внимание, особено при хора с нарушен метаболизъм на сярата или страдащи от алергични заболявания - астма, екзема, оток на Квинке. В такива случаи сярата може да причини тежко влошаване.
Диагностична карта.
Серни кристали от Cozzodisi (Агридженто)
С
Ромбична или моноклинна система
Твърдост 2
Относително тегло 2-2.1
Деколтето несъвършено
Конхоидална фрактура
Цвят жълт, кафяв
Цветът на праха е бял
Гланц от катранено до мазен

Самородна сяра - S. Блясъкът е мазен до диамантен, минералът е прозрачен до полупрозрачен. Цветове: жълт, при изветряне става сив или кафяв до черен. Линията е светложълта, счупването е конхоидално, неравномерно. Много крехък. Деколтето е несъвършено. Сярата се образува като продукт на вулканични сублимати и също се намира в биогенни седиментни отлагания.
Кристалите (ромбична система) са пирамидални, бъчвовидни. Ставите са чести. Агрегатите са твърди, едрозърнести, плътни, понякога землисти (има гроздовидни и бъбрековидни изхвърляния), прахообразни отлагания. Използва се за приготвяне на сярна киселина, в каучуковата промишленост и за борба с вредителите в земеделието. Места на разпространение: остров Сицилия (Италия), Испания. Полша, ОНД, Япония, бр. Луизиана (САЩ), Мексико.
Сярата е пример за полиморфизъм. В стабилната фаза (до 95 o C) орторомбичната система, в интервала до 119 o C, става моноклинна. Той се топи с повишаване на температурата. В природата поради това се среща главно в ромбична форма. Сярата образува бипирамидални кристали и гранулирани агрегати. Характерният цвят на този минерал е лимоненожълт, който може да премине в почти черен поради замърсяване с битум.

Сяра (жълта). Остров Гуам, Тихия океан, САЩ. 10 см. Снимка: A.A. Евсеев.
 Сярата (английски Sulphur, френски Sufre, немски Schwefel) в естествения си вид, както и под формата на серни съединения, е известна от древността. Човекът вероятно се е запознал с миризмата на горяща сяра, задушаващия ефект на серния диоксид и отвратителната миризма на сероводород още в праисторически времена. Приблизително половината от световното производство на сяра идва от природни резерви.
Сярата (английски Sulphur, френски Sufre, немски Schwefel) в естествения си вид, както и под формата на серни съединения, е известна от древността. Човекът вероятно се е запознал с миризмата на горяща сяра, задушаващия ефект на серния диоксид и отвратителната миризма на сероводород още в праисторически времена. Приблизително половината от световното производство на сяра идва от природни резерви.
Диагностични признаци.
Чуплив, лош проводник на топлина; Понякога едно докосване на ръката е достатъчно, за да накара кристала да се напука. Зарежда се с електричество при триене. Топи се при ниска температура и гори във въздуха, отделяйки токсичен газ от серен анхидрид.
Произход.
Сярата е минерал, характерен за седиментни отлагания като изпарители и директна („суха“) вулканична сублимация, както и елемент от вулканични (термални) серни извори (отровни води и горещи изпарения на сяра и киселина). Смята се, че се образува при разлагането на сулфати, предимно гипс (с който най-често се среща заедно), под въздействието на бактерии, предимно "тиобактерии". Моноклинната фаза се образува по време на сублимацията на парите на сярна киселина във вулканична среда (в солфатари). Снимката показва агрегати от серни кристали, обикновено наричани „серни цветя“.
Депозити и приложения.
Големи находища на сяра са открити в Тексас и Луизиана в покрива на солени куполи (евапоритни отлагания), покрити с глинести слоеве. Сярата в тези находища практически няма примеси, тя се извлича чрез пробиване на кладенци, в които се инжектира вряща вода. Той разтопява сярата, която след това се изпомпва на повърхността (Flash метод).
Сярата също е често срещана в Италия по протежение на разкритията на пластовете, съдържащи гипсова сяра, които очертават Апенините, особено в Романя, Марке, Калабрия и Сицилия. Сярата там е наслоена с глинести скали, така че нейното извличане (което вече е прекратено) изисква доста сложен метод. В серните мини на Сицилия са използвали метода на екструзия. Сярата, извлечена от мината, беше разтопена и излята в големи контейнери.


Други находища са известни в Япония и Индонезия. В Италия много красиви кристали от ромбична сяра са известни от Романя, Марке (Пертикара) и Сицилия, където се свързват с целестин и арагонит. Моноклинна сяра е установена в Кампи Флегери и на остров Вулкано. Сярата се използва в химическата промишленост и за производството на минерални торове.

Сяра (кристал). Сицилия, Италия. 5х2,5 см. Снимка: А.А. Евсеев.

Четка от серни кристали (60х40 см) от остров Сицилия (Италия). Снимка: V.I. Дворядкин.

Сяра. Друза от бипирамидални кристали върху кристал от безцветен гипс
и вътре в него. Сицилия, Италия. Снимка: A.A. Евсеев.
Сярата е „минерал на красотата“ (шега в съветските „зони“, 1939-1969 г. на 20 век, където затворниците са били подлагани на сяра, наред с други неща). Съдържанието на сяра в тялото на възрастен е около 0,16% (110 g на 70 kg телесно тегло). Сярата се намира във всички тъкани на тялото, много от нея е в мускулите, скелета, черния дроб, нервната тъкан, кръвта - активен метаболизъм. Повърхностните слоеве на кожата са богати на жълта сяра, където сярата е част от кератина и меланина. Това са сулфиди. Сярата влиза в тялото с хранителни продукти, като част от неорганични и органични съединения. По-голямата част от сярата влиза в тялото като част от аминокиселините.
Основните прояви на излишък на сяра: сърбеж, обрив, фурункулоза, зачервяване и подуване на конюнктивата; появата на малки точкови дефекти на роговицата; болка във веждите и очните ябълки, усещане за пясък в очите; фотофобия, сълзене, обща слабост, главоболие, виене на свят, гадене, катар на горните дихателни пътища, бронхит; загуба на слуха, храносмилателни разстройства, диария, загуба на тегло; анемия, психични разстройства, намалена интелигентност. Сяра - вулкани и серни извори, изпарение на сяра (99,3%). Натрупвайте - продукти. Един източник на прекомерен прием на сяра са съединенията, съдържащи сяра (сулфити), а нарастващата консумация на сулфити е отговорна за увеличаването на случаите на бронхиална астма.
Признаци на недостиг на сяра: запек, алергии, тъпота и косопад, чупливи нокти, високо кръвно налягане, болки в ставите, тахикардия, висока кръвна захар и високи нива на триглицериди в кръвта. Омазняване на черния дроб, кръвоизливи в бъбреците, нарушения на протеиновия и въглехидратния метаболизъм, превъзбуждане на нервната система, раздразнителност. Сярата е минералът, който прави чесъна „цар на растенията“.
Серните атоми са неразделна част от молекулите на незаменимите аминокиселини (цистин, цистеин, метионин), хормони (инсулин, калцитонин), витамини (биотин, тиамин), глутатион, таурин и други важни за организма съединения. В техния състав сярата участва в окислително-възстановителни реакции, процеси на тъканно дишане, производство на енергия, предаване на генетична информация и изпълнява много други важни функции. Сярата е компонент на структурния протеин колаген. Хондроитин сулфатът присъства в кожата, хрущялите, ноктите, връзките и миокардните клапи. Съдържащите сяра метаболити са хемоглобин, хепарин, цитохроми, фибриноген и сулфолипиди.
Сярата се екскретира в урината под формата на неутрална сяра и неорганични сулфати, по-малка част от сярата се екскретира през кожата и белите дробове и се екскретира главно в урината под формата на SO42–. Ендогенната сярна киселина, образувана в организма, участва в неутрализирането на токсични съединения (фенол, индол и др.), Произведени от чревната микрофлора, а също така свързва чужди за тялото вещества, включително лекарства и техните метаболити. В този случай се образуват безвредни съединения - конюгати, които след това се екскретират от тялото. Метаболизмът на сярата се контролира от тези фактори, които имат регулаторен ефект върху протеиновия метаболизъм (хормони на хипофизата, щитовидната жлеза, надбъбречните жлези, половите жлези).
ADR 2.1
Запалими газове
Риск от пожар. Риск от експлозия. Може да е под натиск. Риск от задушаване. Може да причини изгаряния и/или измръзване. Контейнерите могат да експлодират при нагряване (изключително опасно - практически не горят)
ADR 2.2
Газова бутилкаНезапалими, нетоксични газове.
Риск от задушаване. Може да е под натиск. Те могат да причинят измръзване (подобно на изгаряне - бледност, мехури, черна газова гангрена - скърцане). Контейнерите могат да експлодират при нагряване (изключително опасно - експлозия от искра, пламък, кибрит, практически не горят)
Използвайте прикритие. Избягвайте ниски площи (дупки, низини, окопи)
Зелен диамант, ADR номер, черна или бяла газова бутилка (цилиндър, тип термос)
ADR 2.3
Токсични газове. Череп и кръстосани кости
Опасност от отравяне. Може да е под натиск. Може да причини изгаряния и/или измръзване. Контейнерите могат да експлодират при нагряване (изключително опасно - мигновено разпространение на газове в цялата околност)
Използвайте маска, когато напускате превозно средство при спешни случаи. Използвайте прикритие. Избягвайте ниски площи (дупки, низини, окопи)
Бял диамант, ADR номер, черен череп и кръстосани кости
ADR 3
Запалими течности
Риск от пожар. Риск от експлозия. Контейнерите могат да експлодират при нагряване (изключително опасно - изгарят лесно)
Използвайте прикритие. Избягвайте ниски площи (дупки, низини, окопи)
Червен диамант, ADR номер, черен или бял пламък
ADR 4.1
Запалими твърди вещества, самоактивиращи се вещества и твърди десенсибилизирани експлозиви
Риск от пожар. Запалими или горими вещества могат да се възпламенят от искри или пламъци. Може да съдържа самореактивни вещества, които са способни на екзотермично разлагане при нагряване, контакт с други вещества (като киселини, съединения на тежки метали или амини), триене или удар.
Това може да доведе до отделяне на вредни или запалими газове или изпарения или спонтанно запалване. Контейнерите могат да експлодират при нагряване (те са изключително опасни - практически не горят).
Риск от експлозия на десенсибилизирани експлозиви след загуба на десенсибилизатор
Седем вертикални червени ивици на бял фон, еднакви по размер, ADR номер, черен пламък
ADR 8
Корозивни (каустични) вещества
Риск от изгаряне поради корозия на кожата. Могат да реагират бурно един с друг (компоненти), с вода и други вещества. Разлят/разпръснат материал може да отдели корозивни изпарения.
Опасен за водната среда или канализационната система
Бяла горна половина на ромба, черна - долна, еднакви по размер, ADR номер, епруветки, стрелки
| Наименование на особено опасен товар по време на транспортиране | Номер ООН | Клас ADR |
| Серен анхидрид, стабилизиран СЯРЕН ТРИОКСИД, СТАБИЛИЗИРАН | 1829 | 8 |
| Серен анхидрид СЯРЕН ДИОКСИД | 1079 | 2 |
| Въглероден дисулфид | 1131 | 3 |
| СЯРЕН ХЕКСАФЛУОРИД газ | 1080 | 2 |
| ОТРАБОТЕНА СЯРНА КИСЕЛИНА | 1832 | 8 |
| СЯРНА КИСЕЛИНА, ДИМЯЩА | 1831 | 8 |
| СЯРНА КИСЕЛИНА, която съдържа не повече от 51% киселина, или ТЕЧНОСТ ОТ БАТЕРИЙНА КИСЕЛИНА | 2796 | 8 |
| СЯРНА КИСЕЛИНА, РЕГЕНЕРИРАНА ОТ КИСЕЛЕН катран | 1906 | 8 |
| СЯРНА КИСЕЛИНА, която съдържа повече от 51% киселина | 1830 | 8 |
| СЯРНА КИСЕЛИНА | 1833 | 8 |
| СЯРА | 1350 | 4.1 |
| СЯРАТА Е СТОПЕН | 2448 | 4.1 |
| Серен хлорид СЯРЕН ХЛОРИД | 1828 | 8 |
| Серен хексафлуорид СЯРЕН ХЕКСАФЛУОРИД | 1080 | 2 |
| Серен дихлорид | 1828 | 8 |
| СЯРЕН ДИОКСИД | 1079 | 2 |
| СЯРЕН ТЕТРАФЛУОРИД | 2418 | 2 |
| СЯРЕН ТРОКСИД СТАБИЛИЗИРАН | 1829 | 8 |
| СЯРЕН ХЛОРИД | 1828 | 8 |
| Водороден сулфид | 1053 | 2 |
| ВЪГЛЕРОД ДИСУЛФИД | 1131 | 3 |
| БЕЗОПАСНИ КИБРИТИ в кутии, книги, картони | 1944 | 4.1 |
| ПАРАФИН КИБРИЧ “ВЕСТА” | 1945 | 4.1 |
| Парафинови кибрити ПАРАФИНОВИ КИБРИСИ “ВЕСТА” | 1945 | 4.1 |
| МИНИ КИБРИТИ | 2254 | 4.1 |
Камък, минерал, минерали, камъни, кристал, порода, скъпоценни камъни, естествени камъни, скали, скъпоценен камък, скала, див камък, камъни и минерали, име на камъни, естествен камък, естествен камък, минерални камъни, полускъпоценен камък, минерали това са камъни каталог, минералогия, значението на камъните, какво представляват минералите, свойства на камъните, имена на камъни и минерали, имена и снимки на естествени камъни, естествени камъни, минерали камъни, естествени камъни, снимки и имена на камъни, имена на минерали, снимки на див камък, скали и минерали, минерали и камъни, химичният състав на минералите, от какво е направен камъкът, най-невероятните камъни и минерали, списък на минерали, каталог на минерали, камъни и техните свойства, скъпоценни минерали, естествен камък , видове минерали, видове минерали, каменен кристал, свойства на камъка, геология камъни, основни минерали, минерали и тяхната класификация, най-красивите минерали, дефиниция на минерали, произход на камъните, кристален минерал, обикновени камъни, класификация на минералите, описание на камъните, как изглеждат скъпоценните камъни в природата, какво е камък, видове естествен камък, ценен минерал, наука за минералите, химична класификация на минералите, магнитни свойства на минералите, свят на минералите, минерална скала, какви са скалите и минералите, видове камъни, състав на камъните, описание на минерали, камъни в природата, полезни камъни, идентификация на камъни, плътност на минералите, твърдост на скалите, снимки на камъни и техните имена, класификация на минерали, геология, скали и минерали, имена на полускъпоценни камъни и снимки, характеристики на минералите, структура на камъка, минерали в природата.
Сярата е елемент от периодичната таблица на Д. И. Менделеев, нейният атомен номер е шестнадесет. Има неметални свойства. Означава се с латинската буква S. Предполага се, че името има индоевропейски корен - „да горя“.
Историческа перспектива
Не е ясно кога е открита сярата и е започнал нейният добив. Известно е, че древните хора са знаели за него много преди нашата ера. Ранните свещеници са го използвали в своите култови ритуали и са го включвали в смеси за опушване. Минералът сяра се е смятал за продукт, произведен от боговете, които са живели предимно в подземния свят.
Дълго време, както свидетелстват исторически документи, той е бил използван като компонент на запалими смеси, използвани за военни цели. Омир също не пренебрегва минерала сяра. В едно от произведенията си той описва „изпарения“, които имат пагубен ефект върху хората при изгаряне.
Историците предполагат, че сярата е била елемент в така наречения „гръцки огън“, който всявал страх във враговете.
През осми век в Китай започва да се използва за приготвяне на пиротехнически смеси, включително запалими вещества, наподобяващи барут.
През Средновековието той е бил един от трите основни елемента на алхимиците. Те активно използваха минералната самородна сяра в своите изследвания. Това често води до факта, че експериментите с него се приравняват на магьосничество, а това от своя страна води до преследване от страна на инквизицията на древните химици и техните последователи. От тези времена, от Средновековието и Ренесанса, миризмата на горяща сяра и нейните газове започва да се свързва с действията на зли духове и дяволски прояви.
Имоти
Природната минерална сяра има молекулярна решетка, която други подобни елементи нямат. Това води до факта, че има ниска твърдост, липса на разцепване и е доста чуплив материал. Специфичното тегло на сярата е 2,7 грама на кубичен сантиметър. Минералът има лоша електрическа, слаба топлопроводимост и ниска точка на топене. Свети свободно при излагане на открит пламък, включително кибрит, цветът на пламъка е син. Запалва се добре при температури около 248 градуса по Целзий. При изгаряне отделя серен диоксид, който има остра задушлива миризма.

Описанията на серния минерал са разнообразни. Има нюанси на светло жълто, слама, мед, зеленикаво. Сярата, която има органични вещества в структурата си, има кафяв, сив или черен цвят. На снимката минералът сяра в своята твърда, чиста, кристална форма винаги привлича окото и е лесно разпознаваем.
Вулканичната сяра е ярко жълта, зеленикава, оранжева. В природата можете да го намерите под формата на различни маси, плътни, земни, прахообразни. Кристални обрасли серни кристали също се срещат в природата, но доста рядко.
Сярата в природата
Естествената сяра рядко се среща в чисто състояние. Но в земната кора запасите му са много значителни. Това са предимно руди, в които серните слоеве присъстват в големи количества.

Досега науката не е установила причината за появата на серни отлагания. Някои версии са взаимно изключващи се. Като се има предвид, че сярата проявява висока химическа активност, се предполага, че при формирането на повърхността на земната кора тя многократно е била свързвана и освобождавана. Как протичат тези реакции не е установено със сигурност.
Според една версия се предполага, че сярата е следствие от излугването на сулфати, които са станали отпадъчни продукти на отделни бактерии. Последните използват минерални съединения като храна.
Изследователите разглеждат различни версии на процесите на заместване на сярата в земната кора, които водят до нейното освобождаване и натрупване. Но все още не е възможно ясно да се разбере естеството на възникването му.
Физични и химични свойства на сярата
Първите научни изследвания са проведени едва през 18 век. Задълбочено изследване на свойствата на серния минерал е извършено от френския учен Антоан Лавоазие. Така той установява, че кристализира от стопилка, като първоначално приема игловидни форми. Тази форма обаче не е постоянна. С понижаване на температурата сярата рекристализира, образувайки обемни полупрозрачни образувания с лимоненожълт или златист оттенък.
Находища, добив на сяра
Основният източник на добив на сярния минерал са находищата. Според изчисленията на геолозите, световните й запаси възлизат на около 1,4 милиарда тона.

Древните хора, както и миньорите от Средновековието, са извличали сяра, като са заравяли голям глинен съд в дълбините. Върху него беше поставен друг, който имаше дупка на дъното. Горният контейнер беше пълен със скала, която съдържаше сяра. Тази структура беше отоплена. Сярата започна да се топи и да тече в долния съд.

Понастоящем добивът се извършва чрез открит добив, както и чрез използване на методи за топене под земята.
На територията на Евразия има големи находища на сяра в Туркменистан, Поволжието и други места. Значителни залежи в Русия са открити на левия бряг на река Волга, която се простира от Самара до Казан.
При разработването на серен минерал се обръща специално внимание на безопасността. Това се дължи на факта, че рудата винаги е придружена от натрупване на сероводород, което е много вредно за дишането. Самият минерал има способността да се запалва и да образува експлозивни съединения.
Най-разпространеният метод за добив е откритият. В този случай горната част на скалите се отстранява с минно оборудване. Взривните операции раздробяват рудната част. След това фракциите се изпращат в предприятието за процеса на обогатяване, а след това в заводите за топене, за да се получи чиста сяра.
Ако минералът е дълбок и обемът му е значителен, за извличане се използва методът на Фраш.
В края на 1890 г. инженерът Фраш предлага да се стопи сярата под земята и след като се превърне в течно състояние, да се изпомпва. Този процес е сравним с производството на нефт. Като се има предвид доста ниската идея на инженера, той беше успешно тестван и промишленото извличане на този минерал започна по този начин.

През втората половина на 20-ти век започва активно да се използва методът за извличане чрез използване на високочестотни токове. Тяхното въздействие също води до топене на сярата. Последващото инжектиране на сгъстен горещ въздух позволява да се ускори издигането му в течно състояние до повърхността.
Сярата се намира в големи количества в природните газове. За извличането му е подходящ методът на Клаус. Използват се специални серни ями, в които се извършва дегазация. Резултатът е твърд модифициран продукт с високо съдържание на сяра.
Приложение
Около половината от цялата добита сяра се използва за производството на сярна киселина. Този минерал е необходим и за производството на каучук, лекарства и като фунгициди в селското стопанство. Минералът е намерил приложение и като конструктивен елемент в популярния заместител на серен асфалт и портландцимент - серен бетон. Те се използват активно в производството на различни пиротехнически състави и в производството на кибрит.
Биологична роля
Сярата е важен биогенен елемент. Той е част от значителен брой аминокиселини. Компонент в образуването на протеинови структури. При бактериалната фотосинтеза минералът участва в окислително-възстановителните реакции на организма и е източник на енергия. В човешкото тяло има около два грама сяра на килограм тегло.
Сярата в чистата си форма не е токсично вещество, за разлика от летливите газове, които включват анхидрид, сероводород и т.н.
Пожарни свойства
Сярата е пожароопасен минерал. Неговите фино смлени фракции са способни на самозапалване при наличие на влага, при контакт с окислители, както и при създаване на смеси с въглища, мазнини и масла. Сярата се гаси с пръскана вода и въздушно-механична пяна.
Описание и свойства на сярата
Сярае вещество, което е в група 16, под третия период и има атомен номер 16. Може да се намери както в естествена, така и в свързана форма. Сярата се обозначава с буквата S. Известен сярна формула– (Ne)3s 2 3p 4 . Сярата като елемент е включена вмного протеини.
Снимката показва кристали сяра
Ако говорим за атомна структура на елемента сяра, тогава във външната му орбита има електрони, чието валентно число достига шест.
Това обяснява свойството на елемента да бъде максимално шествалентен в повечето комбинации. В структурата на природния химичен елемент има четири изотопа и това са 32S, 33S, 34S и 36S. Говорейки за външната електронна обвивка, атомът има схема 3s2 3p4. Радиусът на атома е 0,104 нанометра.
Свойства на сяратасе разделят основно на физически типове. Това включва факта, че елементът има твърд кристален състав. Две алотропни модификации са основното състояние, в което този серен елемент е стабилен.
Първата модификация е ромбична, лимоненожълта на цвят. Стабилността му е по-ниска от 95,6 °C. Вторият е моноклинен, с меденожълт цвят. Неговата устойчивост варира от 95,6 °C до 119,3 °C.

Снимката показва минералната сяра
По време на топенето химическият елемент се превръща в подвижна течност, която е жълта на цвят. Става кафяво, достигайки температури над 160 °C. И то при 190°C цвят на сяратасе превръща в тъмно кафяво. След достигане на 190 °C се наблюдава намаляване на вискозитета на веществото, което въпреки това става течно след нагряване до 300 °C.
Други свойства на сярата:
Практически не провежда топлина или електричество.
Не се разтваря при потапяне във вода.
Разтворим е в амоняк, който има безводна структура.
Също така е разтворим във въглероден дисулфид и други органични разтворители.
ДА СЕ характеристики на елемента сяраважно е да добавите неговите химически характеристики. Тя е активна в това отношение. Ако сярата се нагрее, тя може просто да се комбинира с почти всеки химичен елемент.

Снимката показва проба сяра, добита в Узбекистан
С изключение на инертните газове. При контакт с метали, химикали. елементът образува сулфиди. Стайната температура позволява на елемента да реагира с. Повишената температура повишава активността на сярата.
Нека разгледаме как се държи сярата с отделни вещества:
При металите е окислител. Образува сулфиди.
Активно взаимодействие протича с водорода при високи температури - до 200 °C.
С кислород. Оксидите се образуват при температури до 280 °C.
С фосфор, въглерод - той е окислител. Само ако няма въздух по време на реакцията.
С флуора действа като редуциращ агент.
С вещества, които имат сложна структура - също като редуциращ агент.
Отлагания и производство на сяра
Основният източник за получаване на сяра са нейните находища. Общо в света има 1,4 милиарда тона запаси от това вещество. Добива се както чрез открит и подземен добив, така и чрез подземно топене.

Снимката показва добива на сяра във вулкана Кава Иджен
Ако важи последният случай, тогава се използва вода, която е прегрята и топи сярата с нея. В нискокачествените руди елементът се съдържа в приблизително 12%. Богат – 25% и повече.
Често срещани видове депозити:
Стратиформен – до 60%.
Солен купол – до 35%.
Вулканогенни – до 5%.
Първият тип е свързан със слоеве, наречени сулфатно-карбонатни. В същото време в сулфатни скали се намират рудни тела с дебелина до няколко десетки метра и размери до стотици метри.
Също така тези пластови отлагания могат да бъдат намерени сред скали със сулфатен и карбонатен произход. Вторият тип се характеризира със сиви отлагания, които са ограничени до солени куполи.
Последният тип се свързва с вулкани, които имат млада и модерна структура. В този случай рудният елемент има листовидна форма с форма на леща. Може да съдържа сяра в размер на 40%. Този тип депозити са често срещани в тихоокеанския вулканичен пояс.
Депозит на сярав Евразия се намира в Туркменистан, Поволжието и други места. Сярни скали се намират близо до левия бряг на Волга, който се простира от Самара. Ширината на скалната ивица достига няколко километра. Освен това те могат да бъдат намерени чак до Казан.

Снимката показва сяра в скала
В Тексас и Луизиана огромни количества сяра се намират в покривите на солени куполи. Особено красиви италианци от този елемент се намират в Романя и Сицилия. А на остров Вулкано намират моноклинна сяра. Елементът, който е окислен от пирит, е открит в Урал в района на Челябинск.
За копаене сяра химически елементизползвайте различни методи. Всичко зависи от условията на възникването му. В същото време, разбира се, се обръща специално внимание на безопасността.
Тъй като сероводородът се натрупва заедно със сярната руда, е необходимо да се подходи особено сериозно към всеки метод за добив, тъй като този газ е отровен за хората. Сярата също има склонност да се запалва.
Най-често те използват отворения метод. Така с помощта на багери се отстраняват значителни части от скалите. След това рудната част се раздробява с експлозии. Бучките се изпращат във фабриката за обогатяване. След това - в завода за топене на сяра, където се получава сяра от концентрат.

На снимката се вижда сяра в пристанището, донесена по море
В случай на дълбоко поява на сяра в много обеми се използва методът на Frasch. Сярата се топи още под земята. След това, подобно на петрола, се изпомпва през счупен кладенец. Този подход се основава на факта, че елементът се топи лесно и има ниска плътност.
Известен е и метод за разделяне, използващ центрофуги. Само този метод има недостатък: сярата се получава с примеси. И тогава е необходимо да се извърши допълнително почистване.
В някои случаи се използва методът на сондаж. Други възможности за добив на елемента сяра:
Пара-вода.
Филтриране.
Термичен.
Центробежен.
Екстракция.
Приложение на сяра
По-голямата част от добитата сяра се използва за производството на сярна киселина. И ролята на това вещество е много голяма в химическото производство. Трябва да се отбележи, че за получаване на 1 тон сярно вещество са необходими 300 kg сяра.
Бенгалските огънчета, които светят ярко и имат много багрила, също се правят със сяра. Хартиената промишленост е друга област, в която отива значителна част от извлеченото вещество.

На снимката е сярна маз
По-често прилагане на сяранамира при задоволяване на производствени нужди. Ето някои от тях:
Използване в химическото производство.
За производство на сулфити, сулфати.
Производство на вещества за торене на растения.
За получаване на цветни видове метали.
За придаване на стомана на допълнителни свойства.
За изработка на кибрит, материали за взривове и пиротехника.
С помощта на този елемент се произвеждат бои и влакна от изкуствени материали.
За избелване на тъкани.
В някои случаи серен елементвключени в мехлеми, които лекуват кожни заболявания.
Цена на сярата
Според последните новини необходимостта от сяра активно нараства. Цената на руски продукт е 130 долара. За канадската версия – $145. Но в Близкия изток цените се увеличиха до $8, което доведе до цена от $149.

Снимката показва голям екземпляр от минерала сяра
В аптеките можете да намерите смлян прах от сяра на цена от 10 до 30 рубли. Освен това има възможност за закупуване на едро. Някои организации предлагат закупуване на гранулирано техническо оборудване на ниска цена. газ сяра.
/ минерал Sulphur Native
Самородната сяра е често срещан минерал от класа на самородните елементи. Сярата е пример за добре дефиниран енантиоморфен полиморфизъм. В природата образува 2 полиморфни модификации: a-орторомбична сяра и b-моноклинна сяра. При атмосферно налягане и температура 95,6°C a-сярата се превръща в b-сяра. Разновидност: вулканит (селенова сяра). Оранжево-червен, червено-кафяв цвят. Произходът е вулканичен. Самородната сяра се характеризира с: неметален блясък и това, че сярата се запалва с кибрит и гори със син пламък, отделяйки серен диоксид, който има остра задушлива миризма. Най-характерният цвят на самородната сяра е светложълт. Лесно разтворим в канадски балсам, терпентин и керосин. Неразтворим във вода, но разтворим в CS2. Неразтворим в HCl и H2SO4. HNO3 и царската вода окисляват сярата, превръщайки я в H2SO4. Сярата се образува по време на вулканични изригвания, по време на изветряне на сулфиди, по време на разлагане на гипсоносещи седиментни слоеве, а също и във връзка с дейността на бактериите. Основните видове залежи на самородна сяра са вулканогенни и екзогенни (хемогенно-седиментни). Преобладават екзогенните находища; те са свързани с гипсови анхидрити, които под въздействието на емисиите на въглеводороди и сероводород се редуцират и заменят със сярно-калцитни руди. Всички големи находища имат такъв инфилтрационно-метасоматичен генезис. Често се образува естествена сяра (с изключение на големи натрупвания) в резултат на окисляването на H2S. Геохимичните процеси на неговото образуване се активират значително от микроорганизми (сулфатредуциращи и тионни бактерии). Сред вулканогенните отлагания на естествена сяра основните са хидротермално-метасоматични (например в Япония), образувани от сяросъдържащи кварцити и опалити и вулканогенно-седиментни сяраносещи тини на кратерни езера. Образува се и по време на фумаролна активност. Образувана в условията на земната повърхност, самородната сяра все още не е много стабилна и, постепенно окислявайки се, поражда сулфати, гл. като мазилка. Понякога по време на вулканични процеси сярата се изхвърля в течна форма. Това се случва, когато сярата, отложена преди това по стените на кратерите, се стопи с повишаване на температурата. Сярата също се отлага от горещи водни разтвори в резултат на разлагането на сероводород и серни съединения, освободени по време на една от по-късните фази на вулканичната активност. Тези явления сега се наблюдават близо до отворите на гейзерите в Йелоустоун Парк (САЩ) и Исландия. Среща се заедно с гипс, анхидрит, варовик, доломит, каменни и калиеви соли, глини, битуминозни находища (нефт, озокерит, асфалт) и пирит. Намира се и по стените на вулканични кратери, в пукнатини в лава и туфи, заобикалящи отворите на вулкани, както активни, така и угаснали, близо до серни минерални извори. На територията на Евразия всички промишлени находища на самородна сяра са с повърхностен произход. Някои от тях се намират в Туркменистан, в Поволжието и др. Скали, съдържащи сяра, се простират по левия бряг на Волга от град Самара в ивица, широка няколко километра до Казан. Сярата вероятно се е образувала в лагуните през пермския период в резултат на биохимични процеси. Депозитите на сяра се намират в Раздол (Лвовска област, Карпатски регион), Яворовск (Украйна) и в Урал-Ембински район. В Урал (Челябинска област) се среща сяра, образувана в резултат на окисляването на пирит. Сярата с вулканичен произход се намира в Камчатка и Курилските острови. Основните запаси на сяра на капиталистическите страни се намират в Ирак, САЩ (Луизиана и Юта), Мексико, Чили, Япония и Италия (Сицилия). Биогенна седиментна сяра: Сяра от вулканичен произход: Сяра в сулфидни окислителни зони: Използва се при производството на сярна киселина (около 50% от добитото количество). През 1890 г. Херман Фраш предлага топенето на сяра под земята и извличането й на повърхността чрез кладенци, а в момента серните находища се разработват главно чрез топене на естествена сяра от подземни слоеве директно на нейното местоположение. Сярата също се намира в големи количества в природния газ (под формата на сероводород и серен диоксид); по време на производството на газ тя се отлага по стените на тръбите, което ги прави неработещи, така че се възстановява от газа възможно най-бързо след производство. Сярата се използва широко в химическата, целулозно-хартиената (производство на целулозен сулфат), кожарската и каучуковата промишленост (вулканизация на каучук) и в селското стопанство (производство на пестициди).
Самородната сяра обикновено е представена от a-сяра. Сярата, за разлика от други самородни елементи, има молекулярна решетка, което определя нейната ниска твърдост.Характеристика
Място на раждане
Приложение
докладвайте за грешка в описанието
Свойства на минерала
| Цвят | Чистата сяра е светложълта, с примеси на селен - тъмнокафява, арсен - яркочервена, битум - тъмнокафяв и черен. Известна е млечнобяла и синя сяра. |
| Цвят на щриха | Сламеножълто, бяло |
| произход на името | Думата „сяра“, позната на староруския език от 15 век, е заимствана от старославянската „сера“ - „сяра, смола“, обикновено „запалимо вещество, мазнина“. Етимологията на думата досега не е изяснена, тъй като първоначалното общославянско наименование на веществото е изгубено и думата е достигнала до съвременния руски език в изкривен вид. Според Васмер "сярата" се връща към лат. sera - "восък" или лат. серум - „серум“. Латинската сяра (произлизаща от елинизираното изписване на етимологичния sulpur) вероятно се връща към индоевропейския корен *swelp - „да горя“ |
| Година на откриване | познат от древни времена |
| Състояние на IMA | валиден, описан за първи път преди 1959 г. (преди IMA) |
| Химична формула | S8 |
| Блясък | мазни смола |
| Прозрачност | прозрачен полупрозрачен |
| Деколте | несъвършен от (001) несъвършен от (110) несъвършен от (111) |
| Кинк | конхоидална неравен |
| твърдост | 2 |
| Топлинни свойства | Сярата има ниска точка на топене - 113°C. Гори лесно във въздуха, гори със син пламък, отделяйки задушливи изпарения от серен диоксид (който при взаимодействие с вода образува сярна киселина, която пада като валежи на земята). |
| Типични примеси | Се, Те |
| Strunz (8-мо издание) | 1/0.0-10 |
| Хей CIM Ref. | 1.51 |
| Дана (7-мо издание) | 1.3.4.1 |
| Дана (8-мо издание) | 1.3.5.1 |
| Опции за клетки | a = 10.468Å, b = 12.870Å, c = 24.49Å |
| Поведение | a:b:c = 0,813:1:1,903 |
| Брой формулни единици (Z) | 128 |
| Обем на елементарна клетка | V 3,299.37 Å |
| Побратимяване | Близнаците на (101), (011), (110) са доста редки. |
| Точкова група | mmm (2/m 2/m 2/m) - Дипирамидален |
| Космическа група | Fddd (F2/d 2/d 2/d) |
| Отделност | отделете от (111) |
| Плътност (изчислена) | 2.076 |
| Плътност (измерена) | 2.07 |
| Плеохроизъм | видими |
| Дисперсия на оптичната ос | относително слабо r |
| Показатели на пречупване | nα = 1,958 nβ = 2,038 nγ = 2,245 |
| Максимално двойно пречупване | δ = 0,287 |
| Тип | двуосно (+) |
| ъгъл 2V | измерено: 68°, изчислено: 70° |
| Оптичен релеф | много висок |
| Форма за избор | Образува пресечено-бипирамидални, по-рядко бипирамидални, пинакоидни или дебелопризматични кристали, както и плътни криптокристални, конфлуентни, зърнести и по-рядко фино-влакнести агрегати. Основните форми в кристалите: дипирамиди (111) и (113), призми (011) и (101), пинакоид (001). Също така сраствания и друзи от кристали, скелетни кристали, псевдосталактити, прахообразни и земни маси, отлагания и лепила. Кристалите се характеризират с множество паралелни сраствания. |
| Класове по таксономия на СССР | Неметали |
| IMA класове | Родни елементи |
| сингония | ромбичен |
| Чупливост | да |
| изгаряне | да |
| Литература | Ареис В.Ж. Разработване на находища на самородна сяра чрез подземно топене. - М., 1973 Отлагания на вулканична сяра и някои проблеми на образуването на хидротермални руди. - М., 1971 Геохимия и минералогия на сярата, М., 1972 |
Каталог минерали