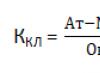IHD morfoloģiskais pamats vairāk nekā 95-97% gadījumu ir koronāro artēriju (CA) ateroskleroze. Aterosklerozes plāksnes, kas sašaurina koronāro asinsvadu lūmenu, lokalizējas galvenokārt proksimālajās koronārajās artērijās, galvenokārt to mutes rajonā. Intramurālie koronārie asinsvadi paliek makroskopiski neskarti. Kreisās koronārās artērijas priekšējais interventrikulārais atzars (LAD LCA) apgādā visu LV priekšējo sienu un lielāko daļu IVS. LMCA (LCB) cirkumfleksais atzars nodrošina asins piegādi LV sānu un mugurējo sienām, un labā koronārā artērija (RCA) nodrošina LV aizmugurējo diafragmas sienu, IVS un RV bazālo daļu, kā arī AV mezgls. Aterosklerozes izmaiņas koronārajā gultnē izraisa pārejošu vai pastāvīgu išēmiju un citas sekas, ko izraisa koronārās asinsrites traucējumi skartajā artērijā.
Trīs lielāko koronāro artēriju (LAD, OB un RCA) aterosklerozes sašaurināšanās pakāpe pacientiem ar koronāro artēriju slimību nav vienāda. Bojājums vienam no tiem (LAD, OB vai RCA) tiek konstatēts aptuveni 30% gadījumu, divas CA - vēl trešdaļai pacientu, bet trīs CA - pārējiem pacientiem. 2/3 pacientu ar koronāro artēriju slimību ar koronāro angiogrāfiju (autopsiju) var atklāt 2-3 koronāro artēriju asinsvadu bojājumus, kam ir visnopietnākā prognoze. Visbiežāk tiek skarta LAD, kas apgādā ievērojamu daļu LV. Traucētai asins plūsmai LAD ir augsts MI un pēkšņas nāves risks. Vēl smagāka prognoze tiek novērota ar aterosklerozes sašaurināšanos vai kreisās artērijas stumbra oklūziju.
Sirds sindroms X
10-15% pacientu ar tipisku koronāro artēriju slimības klīnisko ainu un pārbaudāmām objektīvām pārejošas miokarda išēmijas pazīmēm acīmredzama lielo proksimālo koronāro artēriju aterosklerozes sašaurināšanās netiek konstatēta. Šo IHD gaitas variantu sauc par “X sindromu”. Tās rašanās ir saistīta ar mazo koronāro artēriju bojājumiem, kas koronārās angiogrāfijas laikā netiek vizualizēti. Ārzemju literatūrā kā salīdzinoši reti IHD cēloņi tiek nosauktas dažas slimības un sindromi, ko pavada sirds muskuļa išēmiski bojājumi: iedzimtas koronārās artērijas anomālijas; iekaisīgs koronarīts, ko izraisa koronārās artērijas iesaistīšanās patoloģiskā iekaisuma procesā (nodosa periarterīts, sistēmiskas slimības saistaudi); sifilīts aortīts; krūšu aortas aneirisma sadalīšana; koronārā embolija (ar infekciozu endokardītu, priekškambaru mirdzēšanu, reimatisko sirds slimību); aortas sirds defekti un citi.
Visus šos koronāros bojājumus var pavadīt pārejoša sirds muskuļa išēmija vai pat MI. Tomēr to iekļaušanas IHD jēdzienā piemērotība ir ļoti apšaubāma, jo šai slimībai ir savs skaidri definēts klīniskais un patomorfoloģiskais attēls, kas ļauj atšķirt IHD kā neatkarīgu nosoloģisku vienību. Lielākā daļa uzskaitīto koronāro bojājumu jāuzskata par citu slimību komplikāciju, infekciozu endokardītu ar aortas vārstuļa bojājumu, ko sarežģī LAD trombembolija, attīstoties akūtam miokarda infarktam.
Koronārās sirds slimības riska faktori
Nozīmīgākie no tiem ir: 1. Nemodificējami (nemainīgi) riska faktori: vecums virs 50-60 gadiem; Dzimums Vīrietis); apgrūtināta iedzimtība. 2. Modificēts (maināms): dislipidēmija ( palielināts saturs holesterīna, triglicerīdu un aterogēno lipoproteīnu līmenis asinīs un/vai anti-aterogēnā ABL satura samazināšanās); arteriālā hipertensija(AG); smēķēšana; aptaukošanās; ogļhidrātu metabolisma traucējumi (hiperglikēmija, cukura diabēts); fiziskā neaktivitāte; slikts uzturs; hiperhomocisteinēmija. Tagad ir pierādīts, ka tādiem koronāro sirds slimību riska faktoriem kā dislipidēmija, hipertensija, smēķēšana, aptaukošanās un cukura diabēts ir vislielākā prognostiskā nozīme. Koronārās mazspējas rašanos veicina jebkādu organisku vai funkcionālu faktoru darbība, kas izraisa vai nu tiešu koronārās asinsrites ierobežošanu un perfūzijas spiediena samazināšanos koronārajā sistēmā, vai arī ievērojamu miokarda skābekļa pieprasījuma palielināšanos, ko nepavada. adekvāti palielinot koronāro asins plūsmu.
Pastāv 4 akūtas vai hroniskas koronārās mazspējas mehānismi: 1. Proksimālo koronāro artēriju sašaurināšanās ar aterosklerozes plāksnīti ar koronārās asinsrites un/vai tās funkcionālās rezerves ierobežojumiem un nespēju adekvāti paplašināt koronāros asinsvadus, reaģējot uz koronāro asinsvadu palielināšanos. miokarda skābekļa patēriņš (“fiksēta stenoze”). 2. Smaga koronārā spazma (“dinamiskā stenoze”). 3. Koronāro artēriju tromboze, tai skaitā mikrotrombu veidošanās mikrovaskulārā. 4. Mikrovaskulāra disfunkcija. Vairumā gadījumu pacientiem ar koronāro aterosklerozi rodas vairāku šo mehānismu kombinācija. Koronāro artēriju sašaurināšanās ar aterosklerozes aplikumu (“fiksētā stenoze”) Proksimālās (epikarda) koronārās artērijas progresējoša sašaurināšanās ar aterosklerozes aplikumu izraisa ievērojamu pretestības palielināšanos stenozējošās koronārās artērijas rajonā. Arterioli, kas atrodas distāli no stenozes vietas, kompensējoši paplašinās, samazinās to pretestība (R2), kas pie mērenām stenozes pakāpēm palīdz uzturēt normālu kopējo stenozējošās artērijas koronārā gultnes pretestību (Rtotal) un perfūzijas spiediena vērtību to. Perfūzijas spiediens (AP), zem
kuras darbība veic asins plūsmu neskartā artēriju sistēmā, ir vienāda ar spiediena starpību proksimālajā traukā (P1) un tā distālajās sekcijās (P2): DR = P, - P2.
Stenozējošās koronārās artērijas kopējā koronārā pretestība (Rtotal) sastāv no artērijas proksimālās daļas pretestības (R1), stenozējošās zonas pretestības (Rs) un koronārās gultas distālās daļas pretestības (R2). ). Miera stāvoklī, neskatoties uz koronārās artērijas sašaurināšanos, kas nodrošina ievērojamu pretestību koronārajai asins plūsmai (Rs), Rtot nedaudz palielinās, jo arteriolu un mazo artēriju kompensējošās paplašināšanās dēļ vērtība samazinās. Proksimālās artērijas poststenotiskajā daļā acīmredzamu iemeslu dēļ spiediens (P1) tiek samazināts, bet perfūzijas spiediens (PP) paliek gandrīz tāds pats kā neskartajā koronārajā artērijā, jo strauji samazinās P2.
Palielinoties miokarda skābekļa patēriņam neskartajā koronāro artēriju sistēmā, kurā ir saglabāta koronārā rezerve, ievērojami palielinās arteriolu un mazo artēriju, un ievērojami samazinās artērijas distālās daļas (R2) un Rkopējā pretestības vērtība. . Tā rezultātā palielinās spiediena gradients (DP) un palielinās koronārā asins plūsma. Stenozes zonā uz fizisko aktivitāšu fona un pieaugošās asins plūsmas intensitātes tas palielinās, savukārt R2 vairs nesamazinās, jo mazie asinsvadi ir maksimāli paplašināti un koronārā rezerve ir izsmelta. Rezultātā kopējās pretestības (Rtot) vērtība ievērojami palielinās. Tas noved pie vēl lielāka poststenotiskā spiediena (P1) krituma, vienlaikus saglabājot to pašu P2 vērtību. Tāpēc perfūzijas spiediens (DP) un koronārā asins plūsma samazinās līdz kritiskajam līmenim, un rodas apstākļi miokarda išēmijas rašanās gadījumam.
Šajā koronārās stenozes stadijā intramurālo pretestības asinsvadu kompensējošā paplašināšanās notiek galvenokārt koronārās asinsrites pašregulācijas vielmaiņas mehānismu darbības dēļ, palielināta adenozīna, endotēlija atkarīgā relaksācijas faktora (slāpekļa oksīda - NO), prostaciklīna P012 ražošana. . Tas nodrošina pietiekamu koronārā cirkulācija miera stāvoklī, bet ierobežo koronāro rezervi un pretestības asinsvadu paplašināšanās iespēju, ja tiek pakļauti faktoriem, kas palielina miokarda skābekļa patēriņu.
Šie faktori ietver: 1. Miokarda spriedzes palielināšanos, ko nosaka sistoliskā asinsspiediena līmenis, pēcslodzes apjoms, LV dobuma distālie izmēri un EDP līmenis tajā. 2. Sirdsdarbības ātruma palielināšanās. 3. Paaugstināts sirds muskuļa inotropisms, kas visbiežāk saistīts ar SAS aktivizēšanos un kateholamīnu koncentrācijas palielināšanos asinīs. Šajā slimības attīstības stadijā rodas pārejošas miokarda išēmijas klīniskās un instrumentālās pazīmes ar ievērojamu SAS aktivāciju, fizisku vai emocionālu stresu, sirdsdarbības ātruma palielināšanos un asinsspiediena paaugstināšanos.
Palielinoties proksimālās koronārās artērijas stenozes pakāpei, palielinās kompensējošās vazodilatācijas smagums un tajā pašā laikā samazinās koronārās dilatācijas rezerve. Kad tiek sasniegta kritiskā stenozes pakāpe (75–80% no asinsvada lūmena), asins plūsmas palielināšanās, reaģējot uz pieaugošo miokarda skābekļa patēriņu, kļūst neiespējama. CI pazīmes rodas ar nelielu piepūli, miera stāvoklī. Pie šīs stenozes pakāpes un rezistīvo koronāro asinsvadu maksimālās paplašināšanās koronārās asins plūsmas līmenis kļūst ļoti atkarīgs no intramiokarda spriedzes (vai intraventrikulārā spiediena līmeņa).
Tāpēc jebkurš LV EDP pieaugums, ko izraisa miokarda kontraktilitātes samazināšanās pacientiem ar CHF, LV dobuma paplašināšanās, palielināta priekšslodze, izteikta miokarda hipertrofija vai sirdsdarbības ātruma palielināšanās, izraisa mikrovaskulāras saspiešanas un vēl smagākas slimības. miokarda perfūzijas ierobežojums stenozējošā koronārajā artērijā. Proksimālās koronārās artērijas izteikta stenoze, rezistīvo koronāro asinsvadu maksimāla paplašināšanās, to tālākas paplašināšanās iespējamības samazināšanās un adekvāti palielināts miokarda skābekļa patēriņš ir pirmie mehānismi koronārās mazspējas attīstībai pacientiem ar koronāro artēriju slimību. .
Koronāro artēriju spazmas
Koronāro artēriju spazmas pacientiem ar koronāro artēriju slimību var ietekmēt gan lielos (epikardiālos), gan intramurālos rezistīvos koronāros asinsvadus. Šis svarīgs mehānisms koronārā mazspēja galvenokārt ir saistīta ar koronārās asinsrites vielmaiņas un neirohumorālās regulēšanas pārkāpumiem. Fizioloģiskos apstākļos, reaģējot uz jebkādu sirds muskuļa metabolisma palielināšanos un miokarda skābekļa pieprasījuma palielināšanos, no endotēlija atkarīgs relaksācijas faktors (slāpekļa oksīds - NO) un prostaciklīns POB, kam ir spēcīga vazodilatējoša iedarbība un antiagreganta īpašības, tiek atbrīvots no endotēlija. asinsvadu endotēlija šūnas. Tā rezultātā paplašinās intramurālās rezistīvās koronārās artērijas (arteriolas) un palielinās koronārā asins plūsma, nodrošinot adekvātu miokarda perfūziju paaugstināta miokarda skābekļa pieprasījuma apstākļos. Koronāro asinsvadu kompensējošā relaksācija, ko izraisa adenozīns, bradikinīns, viela P, acetilholīns un citi tiešie vazodilatatori, arī ir no endotēlija atkarīga reakcija.
Pamats koronāro asinsvadu adekvātai fizioloģiskai reakcijai uz jebkādu sirds muskuļa metabolisma palielināšanos ir normāla asinsvadu endotēlija darbība. Tāpēc endotēlija bojājumiem, kas dabiski tiek novēroti pacientiem ar koronāro aterosklerozi, hipertensiju, cukura diabētu, hiperlipidēmiju, aptaukošanos, ir divas negatīvas sekas: no endotēlija atkarīgās koronārās artērijas relaksācijas pavājināšanās, kas galvenokārt saistīta ar sirds mazspējas samazināšanos. slāpekļa oksīda (NO) un prostataciklīna izdalīšanās no endotēlija šūnām; pārmērīga endotēlija vazokonstriktoru vielu (audu angiotenzīna II, endotelīna, tromboksāna A2, serotonīna) ražošana.
Bojātais koronārās artērijas endotēlijs perversi un neadekvāti reaģē uz normāliem hemodinamikas un humorāliem stimuliem. Koronāro artēriju stenozes apstākļos šo situāciju pasliktina būtiskas hemodinamikas izmaiņas aterosklerozes aplikuma zonā (spiediena pazemināšanās un turbulenta asins plūsma poststenotiskajā zonā, spiediena gradienta palielināšanās starp prestenotisko un poststenotisko apgabalu). koronāro artēriju). Tā rezultātā tiek aktivizēts audu angiotenzīnu konvertējošais enzīms (AKE) un strauji palielinās angiotenzīna II izdalīšanās. Tajā pašā laikā palielinās cita spēcīga vazokonstriktora endotelīna ražošana endotēlija šūnās, kas, saistoties ar specifiskiem receptoriem uz gludo muskuļu šūnu membrānas, palielina intracelulārā kalcija koncentrāciju, izraisot ilgstošu un būtisku asinsvadu sieniņu tonis.
POb un NO endotēlija ražošanas samazināšanās pacientiem ar koronāro artēriju slimību izraisa ne tikai koronāro asinsvadu reaktīvās vazodilatācijas nomākšanu, bet arī palielina parietālo trombocītu agregāciju. Tā rezultātā arahidonskābes metabolisma tromboksāna ceļš tiek aktivizēts, pārmērīgi veidojoties tromboksānam A2. Pēdējais izraisa turpmāku trombocītu agregāciju un trombu veidošanos.
Svarīgs iemesls vazokonstriktora reakciju rašanās aterosklerozes koronārajās artērijās ir koronārās asinsrites nervu regulēšanas pārkāpums, ievērojams SAS aktivācijas seku pārsvars un augsta kateholamīnu koncentrācija. Augstākā vērtībašeit ir tieša kateholamīnu vazokonstriktora iedarbība, ko mediē AR adrenerģiskie receptori, kuru ierosināšana izraisa pārsvarā lielo (epikardiālo) A sašaurināšanos. M-holīnerģisko receptoru stimulācijai parasimpātiskās nervu sistēmas aktivācijas laikā ir vazodilatējoša iedarbība. Taču jāņem vērā, ka acetilholīna iedarbību veicina arī koronārās artērijas endotēlijs. Paaugstināts asinsvadu tonuss un koronāro artēriju spazmas pacientiem ar koronāro artēriju slimību ir viens no vadošajiem koronārās mazspējas rašanās mehānismiem.
Veselam cilvēkam normāla trombocītu-asinsvadu un koagulācijas hemostāzes sistēmas darbība nodrošina asinsvadu sieniņas integritātes saglabāšanu. Parasti asiņošana no maziem traukiem, ja tie ir bojāti, apstājas 1-3 minūšu laikā. Tas notiek galvenokārt trombocītu adhēzijas un agregācijas dēļ, kā arī mazākā mērā mikrovaskulāru spazmu dēļ. Sienu bojājumiem ir galvenā loma šajā procesā. asinsvadi un subendotēlija audu kolagēna struktūru iedarbība.
Subendotēlija sastāvā esošā kolagēna (K) un fon Vilebranda faktora (VWF) ietekmē strauji aktivizējas trombocīti, kas, mainot savu formu, uzbriest un veidojot mugurkaula procesus, pielīp (pielīp) pie saistaudu šķiedrām saistaudu malās. brūce. Trombocītu adhēzija (pielipšana) bojāto asinsvadu subendotēlijam ir asinsvadu-trombocītu hemostāzes sākuma stadija un saistīta ar tās trīs komponentu mijiedarbību: 1) trombocītu membrānu specifiskie receptori (glikoproteīns 1b, IIb, IIIa); 2) kolagēns; 3) fon Vilebranda faktors. Pēdējais veido sava veida tiltus starp asinsvadu subendotēlija kolagēnu un trombocītu receptoriem.
ADP, kateholamīnu (CA) un serotonīna, kas izdalās no bojātajām šūnām, ietekmē kolagēns palielina trombocītu agregācijas spēju. Vielas, kas atrodas tā sauktajās elektronu blīvajās trombocītu a-granulās, tiek atbrīvotas no trombocītiem un sāk darboties: liels skaits ADP, serotonīns, adrenalīns, daži proteīni, kas iesaistīti asins agregācijā un koagulācijā (antiheparīna trombocītu faktors IV, P-tromboglobulīni, lamelārais augšanas faktors un daži plazmas koagulācijas faktori - fibrinogēns, V un VIII faktors, kallikreīns, a2-antiplazmīns). Trombocītu iznīcināšanas laikā daži no tiem tiek atbrīvoti svarīgi faktori koagulācija: 1) trombocītu faktors III (tromboplastīns); 2) antiheparīna IV faktors; 3) fon Vilebranda VIII faktors; 4) faktors V; 5) P-tromboglobulīns; 6) dīgļu faktors, a2-antiplazmīns, fibrinogēns.
Trombocīti, kam ir liela ietekme uz lokālās koagulācijas intensitāti un ātrumu trombu veidošanās zonā, mazāk ietekmē asins koagulāciju. Asinsvadu-trombocītu un koagulācijas hemostāze ir savstarpēji saistīti (savienoti), bet tomēr salīdzinoši neatkarīgi procesi. Plazmas un atbrīvoto lamelāro faktoru un audu tromboplastīna mijiedarbības rezultātā sākas asins recēšanas process. Primārās hemostāzes zonā sākotnēji veidojas neliels trombīna daudzums, kas, no vienas puses, pabeidz neatgriezeniskas trombocītu agregācijas procesu, un, no otras puses, veicina fibrīna veidošanos, kas tiek ieausts trombocītu trombā un sablīvē. to. Trombocītu mijiedarbība ar fibrinogēnu tiek veikta, izmantojot specifiskus Pb/Ia receptorus. Svarīga loma trombocītu agregācijas veidošanā ir arahidonskābes atvasinājumiem - prostaglandīniem PCC2 un PON2 un citiem, no kuriem trombocītos veidojas tromboksāns A2, kam piemīt spēcīga agregācijas un vazokonstriktora iedarbība, bet asinsvadu sieniņās - prostaciklīns (PG12). ), kas ir galvenais agregācijas inhibitors.
Pacientiem ar koronāro aterosklerozi trombocītu-asinsvadu hemostāzes aktivācija ir vissvarīgākais koronārās mazspējas rašanās mehānisms. Iemesls tam ir daudzi endotēlija gļotādas defekti. Tas noved pie subendoteliālo struktūru - kolagēna šķiedru, gludo muskuļu šūnu iedarbības. Trombocītu hemostāzes aktivizēšana var izraisīt parietāla tromba veidošanos, distālo koronāro asinsvadu embolizāciju ar atslāņojušiem tromba fragmentiem un ateromatozu aplikumu. Šāda situācija rodas pacientiem ar tā saukto nestabilo stenokardiju un akūtu MI.
Mikrovaskulāra disfunkcija
Mikrovaskulāra disfunkcija ir svarīgs koronārās asinsrites traucējumu mehānisms, kas ir pamatā īpašas koronārās sirds slimības formas - mikrovaskulāras stenokardijas (X sindroma) rašanās pamatā. Mikrovaskulāro disfunkciju raksturo: nav tipisku aterosklerozes izmaiņas lielas (epikarda) CA un izteiktu distālo CA funkcionālo un morfoloģisko traucējumu klātbūtne. Galvenās izmaiņas notiek mazo koronāro artēriju līmenī - prearteriolu, kuru izmērs nepārsniedz 150-350 mikronus. Tiem ir raksturīga ievērojama mazo koronāro artēriju lūmena sašaurināšanās barotnes gludo muskuļu šūnu hipertrofijas un hiperplāzijas un tajā esošo fnbroplastisko procesu dēļ.
IN dažādas jomas miokarda, notiek nevienmērīga prearteriolu sašaurināšanās, to spēja paplašināties samazinās, palielinoties miokarda skābekļa patēriņam.
Šo izmaiņu pamatā ir izteikta endotēlija disfunkcija un palielināta vazokonstriktoru vielu (endotelīna, neiropeptīda Y) ražošana. Samazinās slāpekļa oksīda (NO), prostaciklīna un citu vazodilatējošo vielu ražošana. Attīstās izteikta prearteriolu spazma, parādās pārejošas sirds muskuļa išēmijas zonas. Notiek distālāk izvietotu, neskartu arteriolu paplašināšanās. To pavada starpkoronārais zagšanas sindroms un pieaugoša išēmija. Aprakstīto mikroasinsvadu disfunkciju rašanos veicina trombocītu agregācijas palielināšanās un asins reoloģisko īpašību pasliktināšanās.
Miokarda asins piegādes samazināšanās un kreisā kambara išēmisku bojājumu attīstība (išēmija, distrofija, nekroze) izraisa daudzu funkcionālu un morfoloģisku traucējumu veidošanos sirds muskulī, kas nosaka slimības un tās klīnisko ainu. prognoze. Būtiskākās IHD sekas ir: samazināta enerģijas piegāde kardiomiocītiem; pārziemot ("guļ" un "apdullināts" miokards; kardioskleroze; LV diastoliskā un sistoliskā disfunkcija; ritma un vadīšanas traucējumi.
Samazināta enerģijas piegāde kardiomiocītiem
Parasti pietiekama skābekļa daudzuma klātbūtnē tiek apmierinātas kardiomiocītu enerģijas vajadzības, pateicoties neierobežotai taukskābju un glikozes oksidācijai. Rezultātā veidojas augstas enerģijas fosfāti - adenozīna trifosfāts (ATP) un kreatīnfosfāts (CP), kas tiek izmantoti kardiomiocīta mehānisko, elektrisko un citu funkciju nodrošināšanai. Koronārās asinsrites samazināšanās rada skābekļa deficītu miokardā, un skartās šūnas pāriet uz daudz mazāk efektīvu, anaerobu, vielmaiņas ceļu. Tiek izjaukts oksidatīvās fosforilēšanās process, aktivizējas mazāk efektīva FA oksidēšanās, glikoze pārvēršas laktātā, samazinās šūnu pH, samazinās intracelulārā K' saturs un augstas enerģijas savienojumu veidošanās. Tas noved pie pakāpeniskas šūnas elektriskās aktivitātes samazināšanās, elektrisko impulsu vadīšanas traucējumiem un miokarda mehāniskās funkcijas samazināšanās.
Ir LV išēmisko segmentu lokālās kontraktilitātes pārkāpums (hipokinēzija). Ar pilnīgu koronāro asinsrites pārtraukšanu attīstās kardiomiocītu nekroze. Miokarda nekrotiskajā zonā elektriskās aktivitātes pilnībā nav, elektriskais impulss netiek vadīts, un mehāniskā darbība beidzas (miokarda akinēzija).
Hibernācija (“guļ”) un “apdullināts” miokards
Smagi hroniski koronāro asinsrites traucējumi ne vienmēr izraisa kardiomiocītu nāvi. Atsevišķos gadījumos var novērot divas savdabīgas miokarda reakcijas uz ilgstošu koronārās asinsrites traucējumu esamību: 1. Miokarda ziemošanas fenomens, kas ir hroniskas koronārās perfūzijas samazināšanās apstākļos. 2. “Apdullināšanas” fenomens, kas atklājas pēc sākotnējās audu perfūzijas (reperfūzīna) atjaunošanas.
Miokarda hibernācija (hibernācija - hibernācija) ir LV vietējās kontraktilitātes pārkāpums, kas rodas ar izteiktu un ilgstošu tā perfūzijas samazināšanos, ko nepavada citas išēmijas pazīmes. Hibernācijas fenomens ir unikāla šūnu anabiozes forma, kas nodrošina kardiomiocītu izdzīvošanu skābekļa deficīta apstākļos. Dziļās vielmaiņas izmaiņas, kas rodas hipoksijas laikā (augstas enerģijas savienojumu trūkums, H' jonu uzkrāšanās šūnās un adenozīna un K' jonu izdalīšanās no šūnām), liek kardiomiocītiem krasi ierobežot enerģijas patēriņu un saraušanās funkciju. Pastāv nestabils līdzsvars starp samazinātu perfūziju un samazinātu kontraktilitāti. Miokards ilgstoši saglabā spēju pilnībā atjaunot savu iepriekšējo saraušanās funkciju, ja koronārā asins plūsma normalizējas (veiksmīga trombolīze, revaskularizācija). Turpmāka perfūzijas samazināšanās vai miokarda skābekļa pieprasījuma palielināšanās izraisa išēmijas un nekrozes attīstību.
Hibernējošais miokards reaģē uz kateholamīnu ievadīšanu, nelielu dobutamīna devu ietekmē uz laiku tiek atjaunota miokarda kontraktilitāte, kas apliecina tā dzīvotspēju. “Apdullināta” miokarda parādība (apdullināšana) ir pārejošs pēcišēmisks lokālās LV kontraktilitātes traucējums, kas rodas pēc sākotnējās koronārās cirkulācijas (reperfūzijas) atjaunošanas un išēmijas pārtraukšanas. “Apdullinātajā” miokardā, kas pārdzīvojis ilgstošas išēmijas periodu, atsevišķu kardiomiocītu enerģijas resursi un kontraktilās funkcijas atjaunojas lēnām, vairāku dienu laikā. Neskatoties uz to, ka nav šūnu bojājumu, miokarda kontraktilitāte kādu laiku paliek traucēta. Hibernācijas un “apdullināta” miokarda parādības ir ļoti raksturīgas pacientiem ar koronāro artēriju slimības “paasinājumu” pacientiem ar nestabilu stenokardiju, lai gan tie notiek arī stabilas slimības gadījumā.
Kardioskleroze
Hroniskus miokarda perfūzijas traucējumus un tā metabolisma samazināšanos dabiski pavada kardiomiocītu skaita samazināšanās, to aizstāšana ar jaunizveidotiem saistaudiem, kā arī atlikušo kompensējošās hipertrofijas attīstība. muskuļu šķiedras. Šo morfoloģisko izmaiņu kombinācija kopā ar miokarda išēmiskā bojājuma pazīmēm (miokarda distrofijas un mikronekrozes apgabali) vietējā literatūrā tradicionāli tiek aprakstīta kā difūzā aterosklerotiskā kardioskleroze. Klīniski tas izpaužas ar kreisā kambara sistoliskās un diastoliskās disfunkcijas pazīmēm, lēni progresējošu CHF, kā arī bieži attīstošiem traucējumiem. sirdsdarbība un intraventrikulārā vadīšana (His saišķa kāju un zaru blokāde).
Aterosklerotiskā kardioskleroze pavada citas IHD formas, un mūsdienu starptautiskajā IHD klasifikācijā tā nav izdalīta kā neatkarīga šīs slimības forma. Tomēr tas ievērojami pasliktina slimības gaitu. Saistaudu difūzā proliferācija sirds muskuļos daļēji ir CAS, audu RAS, angiotenzīna I, aldosterona un citu kolagēna veidošanos veicinošu vielu pastiprinātas aktivitātes sekas.
Pacientiem ar MI sirds nekrozes zonas organizēšanas rezultātā veidojas lieli rētu lauki, kas ir pēcinfarkta kardiosklerozes morfoloģiskais pamats. Pēdējais būtiski sarežģī IHD gaitu CHF progresēšanas un augstas pakāpes ventrikulāro aritmiju rašanās dēļ. Ļoti nelabvēlīgas pēcinfarkta kardiosklerozes sekas ir hroniska LV aneirisma - saccular lokāls izspiedums, kas maina koronāro artēriju slimības gaitas raksturu un nosaka slimības prognozi.
Kreisā kambara disfunkcija
LV disfunkcija ir viena no raksturīgās iezīmes raksturīgs daudzām IHD klīniskajām formām. Agri funkcionālie traucējumi sirds muskulis koronāro artēriju slimībā ir LV diastoliskā disfunkcija, ko izraisa: palielināta sirds muskuļa rigiditāte miokarda išēmijas dēļ, aterosklerozes un pēcinfarkta kardiosklerozes klātbūtne, kā arī LV miokarda kompensējošā hipertrofija; ievērojams aktīvās diastoliskās relaksācijas procesa palēninājums, ko izraisa Ca2+ reversās transportēšanas pārtraukšana sarkoplazmas retikulumā un ārpusšūnu vidē. LV sistoliskā disfunkcija attīstās ar smagu augstas enerģijas savienojumu deficītu, un to izraisa aktīna-miozīna mijiedarbības un Ca2′ piegādes pārrāvums kontraktilajiem proteīniem jonu sūkņu bojājumu un augstas enerģijas savienojumu izsīkuma dēļ.
Ritma un vadīšanas traucējumi
Intraventrikulāras un AV blokādes attīstās pacientiem ar koronāro artēriju slimību, galvenokārt difūzās un fokālās kardiosklerozes, kā arī hronisks traucējums asins piegāde AV mezglam un sirds vadīšanas sistēmai. Ventrikulārā un supraventrikulāra ritma traucējumu pamatā ir izteikta sirds muskuļa elektriskā neviendabība, kuras atsevišķas sadaļas atšķiras ar efektīvu ugunsizturīgo periodu ilgumu, kopējo repolarizācijas ilgumu un elektrisko impulsu vadīšanas ātrumu, kas veicina rašanos. agrīnas un vēlīnas depolarizācijas un ierosmes viļņa atkārtotas ienākšanas (atkārtotas ievadīšanas) veidošanās. Augstas pakāpes ventrikulāras aritmijas un letāli vadīšanas traucējumi (III pakāpes AV blokāde, ventrikulāra asistolija) ir visizplatītākie pēkšņas sirds nāves cēloņi pacientiem ar koronāro artēriju slimību.
Koronāro artēriju slimības un miokarda infarkta klīnika, patoģenēze, etioloģija, klasifikācija
Išēmiskā (koronārā) sirds slimība (KSS) ir hroniska slimība, ko izraisa nepietiekama asins piegāde sirds muskulim jeb, citiem vārdiem sakot, tā išēmija. Lielākajā daļā (97-98%) gadījumu IHD ir sirds artēriju aterosklerozes sekas, tas ir, to lūmena sašaurināšanās, ko izraisa tā sauktās aterosklerozes plāksnītes, kas veidojas aterosklerozes laikā uz iekšējām sienām. artērijas. UN
Išēmiska slimība sirds mazspēja ir neatbilstības izpausme starp vajadzību un skābekļa piegādi sirdij. Tas ir atkarīgs no miokarda asinsrites pārkāpuma (koronāro artēriju ateroskleroze) vai no metabolisma izmaiņām miokardā (liels fiziskais vai psihoemocionālais stress, endokrīno dziedzeru slimības utt.). Parasti miokardam ir nepieciešams skābekli un apgādā to ar asinīm ir pašregulējošs process. Ar koronāro sirds slimību šis process tiek traucēts, izraisot skābekļa deficītu sirds muskuļos - stāvokli, ko sauc par miokarda išēmiju.
Galvenā koronārās sirds slimības izpausme ir stenokardijas lēkmes (sarunvalodā stenokardija) - spiedošu sāpju lēkmes aiz krūšu kaula un sirds rajonā, veicot fiziskas aktivitātes. Dažos gadījumos sāpes izplatās uz kreisais plecs, roka, apakšžoklis, dažreiz kopā ar nosmakšanu un gaisa trūkuma sajūtu.
Tā kā koronārā sirds slimība vairumā gadījumu ir koronārās slimības izpausme, kas savukārt ir sirds koronāro artēriju aterosklerozes rezultāts, koronārās sirds slimības profilakse sakrīt ar aterosklerozes profilaksi un ārstēšanu kopumā. Koronārās sirds slimības riska faktori ir iedzimta predispozīcija, vairākas hroniskas slimības (arteriālā hipertensija, cukura diabēts, aptaukošanās u.c.), fizisko aktivitāšu trūkums, smēķēšana, alkohols, vīriešu dzimums u.c. Koronārās sirds slimības profilakse jāsāk nevis pieaugušā un sirmā vecumā, kad parādās pirmās slimības pazīmes, bet gan bērnībā. Visa cilvēka iepriekšējā dzīve nosaka, vai viņam attīstīsies hipertensija, cukura diabēts, ateroskleroze, koronārā mazspēja vai nē.
Nelabvēlīgo psihoemocionālo faktoru nozīme koronārās mazspējas attīstībā parāda nozīmi pareiza izglītība no bērnības visādā ziņā vesels cilvēks.
Tagad ir noskaidrots, ka cilvēki ar augstu holesterīna līmeni asinīs galvenokārt ir uzņēmīgi pret koronāro sirds slimību. Augsts asinsspiediens, cukura diabēts, mazkustīgs dzīvesveids, liekais ķermeņa svars – tas viss liecina par augstu koronārās sirds slimības letālas komplikācijas – miokarda infarkta attīstības draudiem. Miokarda infarkts ir plaši izplatīta un dziļa sirds muskuļa zonas nekroze. Šai smagajai saslimšanai nepieciešama neatliekamā medicīniskā palīdzība, obligāta pacienta hospitalizācija ārstniecības iestādē un neatlaidīga ārstēšanās tur.
Miokarda infarkts ir ārkārtas klīnisks stāvoklis, ko izraisa sirds muskuļa daļas nekroze asins piegādes traucējumu rezultātā. Tā kā pirmajās stundās (un dažkārt pat dienā) no slimības sākuma var būt grūti atšķirt akūtu miokarda infarktu un nestabilu stenokardiju, termins "akūts koronārais sindroms" nesen tiek lietots, lai apzīmētu koronārās sirds slimības paasinājuma periodu. artēriju slimība, kas tiek saprasta kā jebkura klīnisku pazīmju grupa, kas ļauj aizdomām par sirdslēkmes miokardu vai nestabilo stenokardiju. Akūts koronārais sindroms ir termins, kas ir spēkā pirmajā ārsta un pacienta saskarsmē, to diagnosticē, pamatojoties uz sāpēm (ilgstoša stenokardijas lēkme, jauna lēkme, progresējoša stenokardija) un EKG izmaiņām. Ir akūts koronārs sindroms ar ST segmenta pacēlumu vai akūtu pilnīgu kreisā kūļa zara blokādi (stāvoklis, kurā nepieciešama trombolīze un, ja tehniski iespējams, angioplastika) un bez ST segmenta pacēluma - ar tā ST segmenta nomākšanu, inversiju, saplacinātu pseidonormalizāciju. T viļņa vai vispār nav izmaiņu EKG (trombolītiskā terapija nav indicēta). Tādējādi termins “akūts koronārais sindroms” ļauj ātri novērtēt nepieciešamās neatliekamās palīdzības apjomu un izvēlēties adekvātu taktiku pacientu vadīšanai.
Sirds išēmija
Nosūtiet savu labo darbu zināšanu bāzē ir vienkārši. Izmantojiet zemāk esošo veidlapu.
Līdzīgi darbi
Koronāro sirds slimību klasifikācija. Koronāro artēriju slimības attīstības riska faktori. Stenokardija: klīnika; diferenciāldiagnoze. Stenokardijas lēkmes atvieglošana. Ārstēšana interiktālā periodā. Terapeitiskā barošana sirds išēmiskās slimības gadījumā. Koronāro sirds slimību profilakse.
tests, pievienots 16.03.2011
Koronārā sirds slimība, etioloģija un patoģenēze, patoloģiskā anatomija, klīniskā klasifikācija. Individuāla izvēle un pakāpeniska shēma antianginālu zāļu izrakstīšanai pacientiem ar stabilu stenokardiju.
abstrakts, pievienots 03.04.2003
Aterosklerozes etioloģija un patoģenēze, klīniskā gaita, ārstēšanas īpatnības. Galvenās koronārās sirds slimības pazīmes. Slimību veidu klasifikācija. Stenokardija ir vieglākā koronāro artēriju slimības forma. Slimības simptomi, zāles un ārstēšana.
prezentācija, pievienota 01.04.2011
Koronāro sirds slimību, stenokardijas un hroniskas sirds mazspējas pacientu diagnosticēšanas un ārstēšanas iezīmes. Pacienta sūdzību raksturojums, izmeklējumu rezultāti, testi. Slimības etioloģija, patoģenēze un miokarda išēmijas ārstēšana.
slimības vēsture, pievienota 24.03.2010
Koronāro sirds slimību klasifikācija: pēkšņa koronārā nāve, stenokardija, miokarda infarkts, kardioskleroze. Riska faktoru identificēšana. Koronārās sirds slimības patoģenēze. Sirds un asinsvadu sistēmas izpēte. Miokarda infarkta ārstēšana.
abstrakts, pievienots 16.06.2009
Koronāro sirds slimību klīniskā klasifikācija. Stabila stenokardija un tās ekvivalenti. Koronārās išēmijas diennakts ritms. Instrumentālās metodes slimības izpētei. Akūts un nobriedis miokarda infarkts. Kardiogēns šoks un tā ārstēšana.
tests, pievienots 28.08.2011
Riska faktoru ietekme uz koronārās sirds slimības attīstību, tās formām (stenokardija, miokarda infarkts) un komplikācijām. Ateroskleroze kā galvenais koronāro sirds slimību attīstības cēlonis. Traucējumu medikamentozās korekcijas diagnostika un principi.
tests, pievienots 22.02.2010
Koronārā sirds slimība: īpašības un klasifikācija. Stabilas stenokardijas raksturs: klīniskā aina, diagnostika, ārstēšana, profilakse. Akūtas vai hroniskas koronārās mazspējas pamatmehānismi. Slimības riska faktori.
prezentācija, pievienota 03.04.2011
Koronārās sirds slimības klīnisko formu izplatība, dzimums, vecums un sirds slimību psiholoģiskie aspekti. Psihokorekcijas programmas izstrāde cilvēku ar koronāro sirds slimību psiholoģiskās labklājības uzlabošanai.
diplomdarbs, pievienots 20.11.2011
Pacienta sūdzības ievietojot ārstniecības iestādē. Pacienta dzīves un ģimenes vēsture. Sirds un asinsvadu sistēmas izpēte. Klīniskās diagnozes pamatojums: koronārā sirds slimība, stenokardija, priekškambaru mirdzēšana.
slimības vēsture, pievienota 15.02.2014
SIRDS IZĒMIJA
Koronārā sirds slimība ir viena no izplatītākajām slimībām un viens no galvenajiem mirstības, kā arī iedzīvotāju pārejošas un paliekošas invaliditātes cēloņiem attīstītajās pasaules valstīs.Šajā sakarā ir aktuāla I. b. Ar. ieņem vienu no vadošajām vietām starp nozīmīgākajiem medus. 20. gadsimta problēmas Tiek atzīmēts, ka 80. gs. Bija tendence uz mirstības samazināšanos no I. b. Ar. taču, neskatoties uz to, attīstītajās Eiropas valstīs tā veidoja aptuveni 1/2 no kopējās iedzīvotāju mirstības, saglabājot būtisku nevienmērīgu sadalījumu starp dažāda dzimuma un vecuma cilvēku grupām. ASV šajos gados mirstība vīriešiem vecumā no 35-44 gadiem bija apm. 60 uz 100 000 iedzīvotāju, un šajā vecumā mirušo vīriešu un sieviešu attiecība bija aptuveni 5:1. Līdz 65-74 gadu vecumam kopējā mirstība no I. b. Ar. abu dzimumu personas sasniedza vairāk nekā 1600 uz 100 000 iedzīvotāju, un attiecība starp mirušajiem vīriešiem un sievietēm šajā vecuma grupā samazinājās līdz 2:1.
Pacientu liktenis I. b. Ar. kas veido ievērojamu daļu no poliklīniku ārstu novērotā kontingenta, lielā mērā ir atkarīgs no ambulatorās ārstēšanas atbilstības, no tehnisko klīniku diagnostikas kvalitātes un savlaicīguma. slimības formas, kurām nepieciešama neatliekamā palīdzība vai steidzama pacienta hospitalizācija.
Klasifikācija. PSRS izmanto šādu klasifikāciju I. b. Ar. gar ķīli veidlapas, no kurām katrai ir neatkarīga nozīmeķīļa īpašību dēļ. izpausmes, prognozes un elementi terapeitiskā taktika. To 1979. gadā ieteica PVO ekspertu grupa. Klasifikācija katrai galvenajai veidlapai norāda Starptautiskās statistiskās slimību, ievainojumu un nāves cēloņu klasifikācijas IX redakcijas virsraksta numuru.
1. Pēkšņa nāve (primārā sirdsdarbības apstāšanās).
2. Stenokardija.
2. 1. Stenokardija.
2. 1. 1. Jaunā stenokardija.
2.1.2. Stabila stenokardija (norāda funkcionālo klasi no I līdz IV).
2.1.3. Progresējoša stenokardija.
2. 2. Spontāna stenokardija.
2. 3. Nesāpīga (“asimptomātiska”) stenokardija.
3. Miokarda infarkts.
3. 1. Noteikts (neapšaubāms, pierādīts) infarkts (PSRS - lielfokāls).
3. 2. Iespējamais miokarda infarkts (PSRS - mazs-fokāls).
4. Pēcinfarkta kardioskleroze.
5. Sirds ritma traucējumi (norādot formu).
6. Sirds mazspēja (norādot formu un stadiju).
1984. gadā pēc PSRS Medicīnas zinātņu akadēmijas Vissavienības Kardioloģijas pētniecības centra iniciatīvas tika mainītas ar miokarda infarktu saistītās apakšnodaļas. Jo īpaši tā vietā, lai definētu miokarda infarktu kā “pierādītu” un “iespējamu”, ieteicams lietot “liela fokusa” un “maza fokusa”. Pēdējā apakšvirsrakstā ir apvienoti tādi izplatīti apzīmējumi kā “sirdslēkme bez O”. (t.i., ja EKG nav patoloģiska O viļņa), “netransmurāls”, “subendokardiāls”, kā arī forma, ko identificējuši daži ārsti, ko dēvē par “fokālo miokarda distrofiju”. Jēdzienu “iespējamais miokarda infarkts” var izmantot praksē ārkārtas diagnostika ar joprojām neskaidru diagnozi. Šādas situācijas, kā arī progresējoša stenokardija un daži jaunas un spontānas stenokardijas gadījumi dažreiz tiek kombinēti ar terminu “nestabila stenokardija”. Apzīmējumi, kas doti 5. un 6. sadaļā, tiek izmantoti nesāpīgai I. b. gaitai. Ar. ja stenokardijas ekvivalenti ir sirds ritma traucējumi vai elpas trūkuma lēkmes (sirds astma).
Ir nepieņemami formulēt diagnozi I. b. Ar. bez formas atšifrēšanas, jo tādā vispārīgā formā tas nesniedz reālu informāciju par slimības būtību. Pareizi formulētā diagnozē konkrēts ķīlis. forma seko koronārās sirds slimības diagnozei caur resno zarnu, piem. "UN. b. Ar. pirmreizēja slodzes stenokardija”; tajā pašā laikā ķīlis. veidlapa ir norādīta apzīmējumā, ko paredz šīs veidlapas klasifikācija .
Etioloģija es patoģenēze koronārā sirds slimība parasti sakrīt ar etioloģiju un patoģenēzi ateroskleroze. Tomēr ar aterosklerotisko izmaiņu lokalizāciju (koronāro artēriju) un unikālo miokarda fizioloģiju (tā funkcionēšana iespējama tikai ar nepārtrauktu skābekļa un barības vielu piegādi no koronārās asinsrites), kā arī ar atšķirībām individuālā veidošanā. ķīļi. veidlapas I. b. Ar.
Pamatojoties uz daudziem klīniskiem, laboratoriskiem un epidemioloģiskiem pētījumiem, ir pierādīts, ka aterosklerozes, tostarp koronāro artēriju, attīstība ir saistīta ar dzīvesveidu, noteiktu vielmaiņas īpašību un slimību vai patolu klātbūtni indivīdā. apstākļi, kas kopīgi definēti kā riska faktori I. b. Ar. Nozīmīgākie no šiem riska faktoriem ir hiperholesterinēmija, zems holesterīna līmenis asinīs, arteriālā hipertensija, smēķēšana, cukura diabēts, aptaukošanās un I. b. Ar. no tuviem radiniekiem. Slimības varbūtība I. b. Ar. palielinās, kombinējot divus, trīs vai vairākus no uzskaitītajiem riska faktoriem vienam cilvēkam, īpaši ar mazkustīgu dzīvesveidu dzīvi.
Ārstam, kas nosaka profilaktisko un terapeitisko iejaukšanos raksturu un apjomu, svarīga ir gan riska faktoru atpazīšana individuālā līmenī, gan to nozīmīguma salīdzinošs novērtējums. Pirmkārt, ir nepieciešams identificēt aterogēno dislipoproteinēmiju vismaz hiperholesterinēmijas noteikšanas līmenī. . Ir pierādīts, ka tad, kad holesterīna līmenis asins serumā ir no 3,2 līdz 5,2 mmol/l, pastāv nāves risks no I. b. Ar. salīdzinoši mazs. Nāves gadījumu skaits no I. b. Ar. nākamā gada laikā palielinās no 5 gadījumiem uz 1000 vīriešiem ar holesterīna līmeni asinīs 5,2 mmol/l līdz 9 gadījumiem ar holesterīna līmeni asinīs 6,2-6,5 mmol/l un līdz 17 gadījumiem uz 1000 iedzīvotājiem ar holesterīna līmeni asinīs. 7,8 mmol/l. Šis modelis ir raksturīgs visiem cilvēkiem vecumā no 20 gadiem. Atzinums par limita paaugstināšanu pieļaujamo līmeni holesterīna līmenis pieaugušo asinīs, pieaugot vecumam, kā normāla parādība izrādījās neizturama.
Hiperholesterinēmija attiecas uz svarīgi elementi jebkuru artēriju aterosklerozes patoģenēze; jautājums par dominējošās aterosklerozes plāksnīšu veidošanās iemesliem viena vai otra orgāna artērijās (smadzenēs, sirdī, ekstremitātēs) vai aortā nav pietiekami pētīts. Viens no iespējamiem priekšnoteikumiem stenozējošu aterosklerozes plāksnīšu veidošanās koronārajās artērijās var būt to intima muskuļu elastīgās hiperplāzijas klātbūtne (tās biezums var 2-5 reizes pārsniegt barotnes biezumu). Koronāro artēriju intima hiperplāzija, kas konstatēta jau bērnība, var uzskatīt par vienu no faktoriem iedzimta predispozīcija uz koronāro sirds slimību.
Aterosklerozes plāksnes veidošanās notiek vairākos posmos. Sākumā kuģa lūmenis būtiski nemainās. Lipīdiem uzkrājoties aplikumā, rodas tās šķiedrainā apvalka plīsumi, ko pavada trombocītu agregātu nogulsnēšanās, kas veicina lokālu fibrīna nogulsnēšanos. Vieta, kurā atrodas parietālais trombs, ir pārklāta ar jaunizveidotu endotēliju un izvirzās trauka lūmenā, sašaurinot to. Kopā ar lipīdu šķiedru plāksnēm veidojas gandrīz tikai šķiedru stenozes plāksnes, kuras tiek pārkaļķotas.
Katrai plāksnei attīstoties un palielinoties, kā arī palielinoties aplikumu skaitam, palielinās arī koronāro artēriju lūmena stenozes pakāpe, kas lielā mērā (lai gan ne obligāti) nosaka ķīļa smagumu. izpausmes un norise I. b. Ar. Artērijas lūmena sašaurināšanās līdz pat 50% bieži ir asimptomātiska. Parasti skaidrs ķīlis. slimības izpausmes rodas, kad lūmenis sašaurinās līdz 70% vai vairāk. Jo tuvāk atrodas stenoze, jo lielāka miokarda masa tiek pakļauta išēmijai atbilstoši vaskularizācijas zonai. Smagākās miokarda išēmijas izpausmes tiek novērotas ar kreisās koronārās artērijas galvenā stumbra vai mutes stenozi. I. b. izpausmju smagums. Ar. var būt lielāka, nekā paredzēts konstatētajai koronārās artērijas aterosklerozes stenozes pakāpei. Šādos gadījumos miokarda išēmijas izcelsmē var būt krass miokarda skābekļa pieprasījuma pieaugums, koronāro asinsvadu spazmas vai tromboze, kas dažkārt iegūst vadošo lomu patoģenēzē. koronāro artēriju slimība A precizitāte, ir patofiziols. pamatojoties uz I.b. Ar. Priekšnosacījumi trombozei asinsvadu endotēlija bojājuma dēļ var rasties jau aterosklerozes aplikuma attīstības sākumposmā, īpaši tādēļ, ka I. b. Ar. un jo īpaši tās saasināšanās, traucējumu procesi spēlē nozīmīgu lomu hemostāze, galvenokārt trombocītu aktivācija, griezuma iemesli nav pilnībā noskaidroti. Trombocītu adhēzija, pirmkārt, ir sākotnējā saikne asins recekļa veidošanā, kad tiek bojāts endotēlijs vai plīsusi aterosklerozes aplikuma kapsula; otrkārt, tas atbrīvo vairākus vazoaktīvus savienojumus, piemēram, tromboksānu A, trombocītu augšanas faktoru utt. Trombocītu mikrotromboze un mikroembolija var saasināt asinsrites traucējumus stenozējošā traukā. Tiek uzskatīts, ka mikrovaskulārā līmenī normālas asinsrites uzturēšana lielā mērā ir atkarīga no līdzsvara starp tromboksānu un prostatikīnu.
Būtisks artēriju aterosklerozes bojājums ne vienmēr novērš to spazmu.
Skarto koronāro artēriju sērijveida šķērsgriezumu pētījums parādīja, ka tikai 20% gadījumu aterosklerozes plāksne izraisa artērijas koncentrisku sašaurināšanos, kas novērš funkcionālas izmaiņas tās lūmenā. 80% gadījumu tiek konstatēta ekscentriska plāksnes atrašanās vieta, kurā tiek saglabāta asinsvada spēja gan paplašināties, gan spazmas.
Patoloģiskā anatomija. I. b. konstatēto izmaiņu raksturs. Ar. atkarīgs no ķīļa. slimības formas un komplikāciju klātbūtne - sirds nepietiekamība, tromboze, trombembolija uc Izteiktākais morfols. laikā sirds mainās miokarda infarkts un pēcinfarkta kardioskleroze. Kopīgs ķīlis visiem. veidlapas I. b. Ar. ir sirds artēriju aterosklerozes bojājumu (vai trombozes) attēls, ko parasti konstatē lielo koronāro artēriju proksimālajās daļās. Visbiežāk tiek ietekmēts kreisās koronārās artērijas priekšējais interventrikulārais zars, retāk labā koronārā artērija un kreisās koronārās artērijas cirkumfleksais zars. Dažos gadījumos tiek konstatēta kreisās koronārās artērijas stumbra stenoze. Skartās artērijas zonā bieži tiek konstatētas izmaiņas miokardā, kas atbilst tā išēmijai vai fibrozei; izmaiņas raksturo mozaīkas raksts (skartās vietas atrodas blakus neskartām miokarda zonām); kad koronārās artērijas lūmenis ir pilnībā bloķēts, miokardā parasti tiek konstatēta pēcinfarkta rēta. Pacientiem, kuri pārcietuši miokarda infarktu, var konstatēt sirds aneirismu, starpkambaru starpsienas perforāciju, papilāru muskuļu un akordu atdalīšanos un intrakardiālus trombus.
Nav skaidras atbilstības starp stenokardijas izpausmēm un koronāro artēriju anatomiskām izmaiņām, tomēr ir pierādīts, ka stabilai stenokardijai vairāk raksturīgs aterosklerozes plankumu klātbūtne asinsvados ar gludu endotēliju klātu virsmu, savukārt ar progresējošu stenokardiju plāksnītes tiek konstatētas biežāk Arčūlas, plīsumi, sieniņu trombu veidošanās.
Klīnisko formu noteikšana. Diagnozes pamatošanai I. b. Ar. ir nepieciešams galīgi noteikt tā ķīli. forma (no klasifikācijā uzrādītajiem) saskaņā ar vispārpieņemtiem šīs slimības diagnosticēšanas kritērijiem. Vairumā gadījumu diagnozes noteikšanas atslēga ir stenokardijas vai miokarda infarkta atpazīšana - visizplatītākās un tipiskākās I. b. Ar.; cits ķīlis slimības formas ikdienas medicīnas praksē sastopamas retāk un to diagnostika ir grūtāka.
Pēkšņa nāve (primārā sirdsdarbības apstāšanās), domājams, ir saistīta ar miokarda elektrisko nestabilitāti. Uz neatkarīgu formu I. b. Ar. par pēkšņu nāvi uzskata, ja nav pamata diagnosticēt citu I formu. b. Ar. vai cita slimība. Piem. Nāves gadījumi miokarda infarkta agrīnā fāzē nav iekļauti šajā klasē un jāuzskata par nāves gadījumiem no miokarda infarkta. Ja reanimācijas pasākumi netika veiktas vai bija neveiksmīgas, primārais sirds apstāšanās tiek klasificēta kā pēkšņa nāve. Pēdējā tiek definēta kā nāve, kas iestājusies aculiecinieku klātbūtnē uzreiz vai 6 stundu laikā pēc sirdslēkmes sākuma.
Stenokardija kā I. b. izpausmes forma. Ar. apvieno stenokardiju, kas iedalīta jaunatklātā, stabilā un progresējošā, kā arī spontānā stenokardija, kuras variants ir Princmetāla stenokardija.
Stenokardiju raksturo pārejoši sāpju lēkmes krūtīs, ko izraisa fiziska vai emocionāla spriedze vai citi faktori, kas izraisa miokarda metabolisma vajadzību palielināšanos (paaugstināts asinsspiediens, tahikardija). Tipiskos stenokardijas gadījumos sāpes krūtīs (smaguma sajūta, dedzināšana, diskomforts), kas parādās fiziska vai emocionāla stresa laikā, parasti izstaro uz kreisā roka, lāpstiņa. Diezgan reti sāpju lokalizācija un apstarošana ir netipiska. Stenokardijas lēkme ilgst no 1 līdz 10 minūtēm. dažreiz līdz 30 minūtēm, bet ne vairāk. Sāpes, kā likums, ātri izzūd pēc fiziskās slodzes pārtraukšanas vai 2-4 minūtes pēc nitroglicerīna ievadīšanas zem mēles.
Jaunā stenokardija savās izpausmēs un prognozēs ir polimorfa*, tāpēc bez pacienta novērošanas laika gaitā to nevar droši klasificēt kā stenokardiju ar noteiktu gaitu. Diagnoze tiek noteikta laika posmā līdz 3 mēnešiem. no dienas, kad pacients piedzīvoja pirmo sāpju lēkmi. Šajā laikā tiek noteikta stenokardijas gaita: tās regresija, pāreja uz stabilu vai progresējošu.
Stabilas stenokardijas diagnoze tiek noteikta stabilu slimības izpausmju gadījumā, kas izpaužas kā dabiski sāpīgi lēkmes (vai EKG izmaiņas pirms uzbrukuma) ar noteikta līmeņa slodzi vismaz 3 mēnešus. Stabilas stenokardijas smagums raksturo pacienta panesamās fiziskās aktivitātes sliekšņa līmeni, ko izmanto, lai noteiktu tās smaguma funkcionālo klasi, kas jānorāda formulētajā diagnozē (sk. Stenokardija).
Progresējošai stenokardijai raksturīgs salīdzinoši straujš sāpīgu lēkmju biežuma un smaguma palielināšanās ar fiziskās aktivitātes tolerances samazināšanos. Uzbrukumi rodas miera stāvoklī vai ar mazāku stresu nekā iepriekš, tos ir grūtāk apturēt ar nitroglicerīnu (bieži vien jāpalielina tā vienreizēja deva), un dažreiz tie tiek apturēti, tikai ievadot narkotiskos pretsāpju līdzekļus.
Spontāna stenokardija atšķiras no slodzes stenokardijas ar to, ka sāpīgi uzbrukumi rodas bez redzamas saistības ar faktoriem, kas izraisa miokarda metabolisma vajadzību palielināšanos. Uzbrukumi var attīstīties miera stāvoklī bez acīmredzamas provokācijas, bieži naktī vai agrās stundās, un dažreiz tiem ir ciklisks raksturs. Pēc lokalizācijas, apstarošanas, ilguma un nitroglicerīna efektivitātes spontānas stenokardijas lēkmes maz atšķiras no slodzes stenokardijas lēkmēm. Varianta stenokardija jeb Princmetāla stenokardija attiecas uz spontānas stenokardijas gadījumiem, ko pavada pārejošs stenokardijas pieaugums. EKG segments 8T.
Miokarda infarkts. Šī diagnoze tiek noteikta, ja ir klīniski un (vai) laboratoriski (enzīmu aktivitātes izmaiņas) un elektrokardiogrāfiskie dati, kas norāda uz nekrozes fokusa rašanos miokardā, lielu vai mazu. Lielfokāls (transmurāls) miokarda infarkts ir attaisnojams ar patognomoniskām izmaiņām EKG vai specifisku enzīmu aktivitātes palielināšanos asins serumā (noteiktas kreatīnfosfokināzes, laktātdehidrogenāzes u.c. frakcijas) pat ar netipisku ķīli. bilde. Neliela fokāla miokarda infarkta diagnoze tiek veikta, kad 8T segmenta vai T viļņa izmaiņas attīstās dinamikā bez patola. izmaiņas OK8 kompleksā, bet klātesot tipiskām enzīmu aktivitātes izmaiņām .
Pēcinfarkta kardioskleroze. Indikācija pēcinfarkta kardiosklerozei kā komplikācijai I. b. Ar. iekļauts diagnozē ne agrāk kā 2 mēnešus vēlāk. no miokarda infarkta datuma. Pēcinfarkta kardiosklerozes diagnostika kā neatkarīgs ķīlis. veidlapas I. b. Ar. tiek konstatēta, ja stenokardija un citas I. b. formas. Ar. pacientam nav, bet ir fokālās miokarda sklerozes klīniskās un elektrokardiogrāfiskās pazīmes (ilgstoši ritma traucējumi, vadītspēja, hroniska sirds mazspēja, miokarda cicatricial izmaiņu pazīmes EKG). Ja pacienta ilgstošā izmeklēšanas periodā nav konstatētas iepriekšēja infarkta elektrokardiogrāfiskas pazīmes, tad diagnozi var pamatot ar medicīniskiem datiem. dokumentācija, kas saistīta ar akūta miokarda infarkta periodu. Diagnoze norāda uz hrona klātbūtni. sirds aneirisma, iekšējie miokarda plīsumi, disfunkcija papilāru muskuļi tiek noteikta sirds, intrakardiāla tromboze, vadīšanas traucējumu raksturs un sirds ritms, sirds mazspējas forma un stadija.
Koronārās sirds slimības aritmiskā forma, sirds mazspēja kā neatkarīga koronārās sirds slimības forma. Diagnoze pirmās formas, atšķirībā no sirds aritmijas, pavadošā stenokardija, miokarda infarkts vai saistīta ar kardiosklerozes izpausmēm, kā arī tiek noteikta otrās formas diagnoze gadījumos, kad attiecīgi. sirds aritmija vai kreisā kambara sirds mazspējas pazīmes (elpas trūkuma lēkmju veidā, sirds astma, plaušu tūska) rodas kā līdzvērtīgi stenokardijas vai spontānas stenokardijas lēkmēm. Šo formu diagnoze ir sarežģīta un galu galā tiek veidota, pamatojoties uz elektrokardiogrāfiskā pētījuma rezultātu kopumu stresa testos vai monitora novērošanas laikā un selektīvās koronārās angiogrāfijas datiem.
Diagnoze pamatojoties uz analīzi galvenokārt ķīlis. attēlu, ko papildina elektrokardiogrāfiskie pētījumi, kas bieži vien ir pilnīgi pietiekami, lai apstiprinātu diagnozi, un, ja ir aizdomas par miokarda infarktu, arī nosakot virkni asins enzīmu aktivitāti un citus laboratoriskos izmeklējumus. Sarežģītos diagnostikas gadījumos un, ja nepieciešams precizēt sirds un koronāro artēriju bojājumu pazīmes, tiek izmantotas īpašas elektrokardiogrāfijas metodes (testos ar stresu, farmakoloģisko līdzekļu ievadīšanā utt.) un cita veida pētījumi, jo īpaši ehokardiogrāfija. , kontrastvielu un radionuklīdu ventrikulogrāfija, miokarda scintigrāfija un vienīgā uzticamā metode koronāro artēriju stenozes intravitālai noteikšanai ir selektīvā koronārā angiogrāfija.
Elektrokardiogrāfija ir ļoti informatīva metode galveno ķīļu diagnosticēšanai. veidlapas I. b. Ar. EKG izmaiņas patola izskata formā. zobiem PAR vai 08 kombinācijā ar 8T segmenta un T viļņa raksturīgo dinamiku pirmajās stundās un dienās (sk. elektrokardiogrāfija) būtībā ir liela fokusa miokarda infarkta patognomoniskas pazīmes, un to klātbūtne var attaisnot diagnozi, ja nav tipisku ķīļu. izpausmēm. Salīdzinoši specifiskas, novērtējot tās laika gaitā, ir arī izmaiņas 8T segmentā un T viļņā laikā mazs fokālais infarkts un miokarda išēmija, gan kopā ar stenokardijas lēkmi, gan bez tās. Tomēr šo izmaiņu savienojuma ticamība ar išēmiju, nevis ar citu patolu. procesi miokardā (iekaisumi, nekoronāras distrofijas un skleroze), kuros arī tie ir iespējami, ir daudz augstāki, ja tie sakrīt ar stenokardijas lēkmi vai rodas fiziskas slodzes laikā. Tāpēc ar visiem ķīlis. veidlapas I. b. Ar. Elektrokardiogrāfisko pētījumu diagnostisko vērtību palielina stresa un farmakoloģisko testu izmantošana. izmeklējumi (stresa testi netiek izmantoti akūtā miokarda infarkta gadījumā) vai pārejošu (kas raksturīgi īslaicīgai išēmijai) EKG izmaiņu un sirds ritma traucējumu noteikšana, izmantojot Holtera monitorēšanu. No slodzes testiem visizplatītākais ir veloergometra tests ar dozētu slodzi, ko izmanto gan slimnīcās, gan klīnikās, un slimnīcās izmantotā sirds transezofageālā elektrostimulācija. Pharmacol. testus izmanto retāk, un Holtera EKG monitorings kļūst arvien svarīgāks I diagnosticēšanai. b. Ar. ambulatorā veidā.
Veloergometra tests sastāv no nepārtrauktas EKG reģistrēšanas, kamēr pacients min pedāļus ar ierīci, kas imitē velosipēdu un ļauj pakāpeniski mainīt slodzes līmeni un attiecīgi pacienta veiktā darba apjomu laika vienībā, mērot vatos. . Pārbaude tiek pārtraukta, kad pacienti sasniedz t.s. submaksimāls sirdsdarbības ātrums (kas atbilst 75% no tā, kas tiek uzskatīts par maksimālo noteiktā vecumā) vai pirms grafika -: pamatojoties uz pacienta sūdzībām vai patola parādīšanās dēļ. izmaiņas EKG. Par miokarda išēmijas rašanos testa laikā liecina horizontāla vai slīpi lejupejoša 8T segmenta samazināšanās (depresija) vismaz par 1 mm no sākotnējā līmeņa. Tūlīt pēc slodzes apturēšanas 8T segments, kā likums, atgriežas sākotnējā līmenī; šī procesa kavēšanās ir raksturīga pacientiem ar smagu koronāro patoloģiju. Pacienta panesamās slodzes apjoms (slieksnis) veloergometra pārbaudes laikā ir apgriezti proporcionāls koronārās mazspējas pakāpei un stenokardijas smaguma funkcionālajai klasei; jo mazāka šī vērtība, jo lielāku koronāro bojājumu smagumu var pieņemt.
Sirds transezofageālā elektriskā stimulācija, kas panāk dažādas pakāpes paaugstinātu sirdsdarbības ātrumu, tiek uzskatīta par kardioselektīvāku vingrojumu veidu, salīdzinot ar veloergometriju. Tas ir indicēts pacientiem, kuriem tiek veikti vispārējie testi fiziskā aktivitāte Autors dažādu iemeslu dēļ neiespējami. Konkrētākais pozitīvā testa kritērijs ir 8T segmenta samazināšanās (vismaz par 1 mm) pirmajā EKG kompleksā pēc stimulācijas pārtraukšanas.
Pharmacol. testi, kuru pamatā ir EKG izmaiņas, tāpat kā fiziskās aktivitātes laikā, bet dažādu farmakoloģisko līdzekļu ietekmē. Lai noskaidrotu atsevišķu patofiziolu lomu, tiek izmantoti līdzekļi, kas var izraisīt pārejošu miokarda išēmiju. išēmijas izcelsmes mehānismi. Patol. 8T segmenta nobīde EKG testā ar dipirodomolu ir raksturīga saiknei starp išēmiju un tā saukto fenomenu. starpkoronāro zagšanu un testā ar izoproterenolu (β-adrenerģisko receptoru stimulatoru) - ar miokarda metabolisma vajadzību palielināšanos. Spontānas stenokardijas patoģenētiskai diagnostikai īpašos gadījumos izmanto testu ar ergometrīnu, kas var provocēt koronāro artēriju spazmu.
Holtera EKG monitoringa metode ļauj reģistrēt pārejošas aritmijas, 8T segmenta nobīdi un T viļņa izmaiņas dažādos subjekta dabiskās aktivitātes apstākļos (pirms un pēc ēdienreizēm, miega laikā, slodzes laikā utt.) un līdz ar to. identificēt sāpīgas un nesāpīgas pārejošas miokarda išēmijas epizodes, noteikt to skaitu, ilgumu un izplatību dienas laikā, saistību ar fizisko aktivitāti vai citiem provocējošiem faktoriem. Metode ir īpaši vērtīga spontānas stenokardijas diagnosticēšanai, ko nav izraisījusi fiziska aktivitāte.
Ehokardiogrāfijai un kontrastvielu vai radionuklīdu ventrikulogrāfijai ir priekšrocības, diagnosticējot ar koronāro sirds slimību saistītu morfolu. izmaiņas sirds kreisajā kambarī (aneirismas, starpsienas defekti u.c.) un tā kontraktilās funkcijas samazināšanās (samazinot izsviedes frakciju, palielinot diastolisko un beigu sistolisko tilpumu), tai skaitā, lai noteiktu lokālus miokarda kontraktilitātes traucējumus apgabalos. išēmija, nekroze un rētas. Izmantojot ehokardiogrāfija noteikt vairākas sirds patoloģijas formas, tostarp tās hipertrofiju, daudzus sirds defektus, kardiomiopātijas, ar kuru I.b. Ar. dažreiz jums ir jāatšķiras.
Miokarda scintigrāfiju, izmantojot Tc, izmanto, lai noteiktu traucētas pārslodzes zonas, kas scintigrammās redzamas kā radionuklīda uzkrāšanās defekts miokardā. Metode ir visinformatīvākā kombinācijā ar slodzi vai farmakoloģiskiem vingrinājumiem. testi (veloergometrija, transezofageālā stimulācija, testi ar dipiridamolu). Miokarda hipoperfūzijas zonas parādīšanās vai paplašināšanās stresa testa laikā tiek uzskatīta par ļoti specifisku koronāro artēriju stenozes pazīmi. Šo metodi vēlams izmantot, lai diagnosticētu I. b. Ar. gadījumos, kad EKG dinamika fizisko aktivitāšu ietekmē ir grūti novērtējama uz izteiktu sākotnējo izmaiņu fona, piemēram. ar saišķa zaru bloku.
Miokarda scintigrāfiju ar Tc-pirofosfātu izmanto, lai identificētu miokarda nekrozes (infarkta) fokusu, noteiktu tā atrašanās vietu un izmēru. Tiek parādīts, ka patol. radionuklīda uzkrāšanās, kam ir difūzs raksturs, ir iespējama arī ar smagu miokarda išēmiju. Šīs parādības saistību ar išēmiju pierāda fakts, ka pēc veiksmīgas koronāro artēriju šuntēšanas operācijas radionuklīds pārstāj uzkrāties miokardā.
Koronārā angiogrāfija sniedz visdrošāko informāciju par patolu. izmaiņas koronārajā gultā un ir obligāta gadījumos, kad tiek noteiktas indikācijas I. b. ķirurģiskai ārstēšanai. Ar. Metode ļauj identificēt stenozējošas izmaiņas sirds koronārajās artērijās, to pakāpi, atrašanās vietu un apjomu, aneirismu un intrakoronāro trombu (tā saukto sarežģīto aplikumu) esamību, kā arī kolateralu attīstību. Izmantojot īpašus provokatīvus testus, ir iespējams noteikt lielo koronāro artēriju spazmu. Dažiem pacientiem, izmantojot koronāro angiogrāfiju, ir iespējams noteikt kreisā priekšējā interventrikulārā zara anomālo (“niršanas”) atrašanās vietu miokarda biezumā, kura saišķis izplatās pa asinsvadu, veidojot sava veida muskuļu tiltu. Šāda tilta klātbūtne var izraisīt miokarda išēmiju artērijas intramiokarda segmenta saspiešanas dēļ.
Diferenciāldiagnoze tiek veikta starp I. b. Ar. un tās slimības, kuru izpausmes var būt līdzīgas noteikta ķīļa izpausmēm. veidlapas I. b. Ar. - stenokardija, miokarda infarkts, pēcinfarkta kardioskleroze uc Dažos gadījumos, piemēram. ar stenokardiju diferencētu slimību spektrs var būt ļoti plašs, ietverot daudzas sirds, aortas, plaušu, pleiras, perifēro nervu, muskuļu uc slimības, kas izpaužas kā sāpes krūtīs, tostarp tās, kas nav saistītas ar miokarda išēmiju. Citos gadījumos, kad tiek pierādīta miokarda išēmija vai fokālā nekroze, diferencēto slimību klāsts ievērojami sašaurinās, bet neizzūd, jo koronāro artēriju neaterosklerozes bojājumi (ar sistēmisku vaskulītu, reimatismu, sepsi utt.) jāizslēdz išēmijas nekoronarogēnā daba (piemēram, ar sirds defektiem, īpaši ar aortas vārstuļa bojājumiem). Raksturīgs ķīlis. stenokardijas un miokarda infarkta attēls ar to tipiskām izpausmēm, kā arī visa slimības simptomu kopuma holistiska analīze, kas atšķiras no I. b. Ar. vairumā gadījumu ārsts pareizi vada patoloģijas būtību pat sākotnējās diagnostikas stadijā un ievērojami samazina nepieciešamo diagnostikas pētījumu apjomu. Grūtāk ir diferenciāldiagnoze ar netipiskām stenokardijas un miokarda infarkta pazīmēm, kā arī ar ķīli. veidlapas I. b. Ar. izpaužas galvenokārt ar aritmiju vai sirds mazspēju, ja citas pazīmes nav pietiekami specifiskas konkrētai slimībai. Tajā pašā laikā diferencētu slimību klāsts ietver miokardīts. pēcmiokarda kardioskleroze, retas sirds patoloģijas formas (galvenokārt hipertrofiska un paplašināta kardiomiopātija), asimptomātiski sirds defektu varianti, miokarda distrofija dažādas izcelsmes. Šādos gadījumos pacientam var būt nepieciešama hospitalizācija kardioloģijā. slimnīcā, lai veiktu diagnostisko izmeklēšanu, ieskaitot, ja nepieciešams, koronāro angiogrāfiju.
Ārstēšana un sekundārā profilakse koronārā sirds slimība ir vienots pasākumu kopums, tostarp riska faktoru ietekmes uz to novēršana vai samazināšana. Ar. (smēķēšanas izslēgšana, hiperholesterinēmijas samazināšana, arteriālās hipertensijas, cukura diabēta uc ārstēšana); pareizi izvēlēts pacienta fiziskās aktivitātes režīms; racionāla zāļu terapija, jo īpaši lietošana antianginālie līdzekļi, un, ja nepieciešams, arī prot Un voaritmiskas zāles, sirds glikozīdi; koronāro artēriju caurlaidības atjaunošana ar augstu stenozes pakāpi ar operāciju (ieskaitot dažādas endovaskulāras iejaukšanās metodes).
Ārstam jāinstruē pacients ne tikai saistībā ar medikamentu lietošanu, bet arī par visām atbilstošām izmaiņām dzīvesveidā, darba un atpūtas režīmā (ar ieteikumu, ja nepieciešams, mainīt darba apstākļus), pieļaujamo fizisko slodzi. aktivitāte un diēta. Ir nepieciešams noteikt un sadarbībā ar pacientu novērst to faktoru ietekmi uz viņu, kas predisponē viņu uz stenokardijas lēkmi vai izraisa to.
Prasību izvairīties no fiziskas pārslodzes nevar pielīdzināt fizisko aktivitāšu aizliegumam. Gluži pretēji, regulāras fiziskās aktivitātes ir nepieciešamas kā efektīvs līdzeklis I. sekundārajai profilaksei, taču tās ir noderīgas tikai tad, ja nepārsniedz konkrētajam pacientam noteikto slieksni. Tādēļ pacientam savas ikdienas aktivitātes ir jādozē tā, lai novērstu stenokardijas lēkmju rašanos. Regulāri fiziski treniņi (staigāšana, velotrenažieris), nepārsniedzot jaudas robežu, pēc kuras notiek stenokardijas lēkme, pamazām noved pie šī spēka darba veikšanas ar mazāku sirds kontrakciju skaita un asinsspiediena pieaugumu. Turklāt regulāras fiziskās aktivitātes uzlabo pacientu psihoemocionālo stāvokli, veicina labvēlīgas izmaiņas lipīdu vielmaiņā, paaugstina glikozes toleranci, samazina trombocītu agregācijas spēju un, visbeidzot, atvieglo uzdevumu samazināt lieko ķermeņa masu, kad tiek sasniegts maksimālais skābekļa patēriņš laikā. slodze ir lielāka nekā cilvēkam ar normālu ķermeņa svaru.
Diēta pacientam I. b. Ar. parasti ir vērsta uz pārtikas kopējā kaloriju daudzuma ierobežošanu un holesterīnu saturošu pārtikas produktu saturu tajā, ir ieteicams, ņemot vērā pacienta individuālos paradumus un uztura tradīcijas, kā arī blakusslimību un patola klātbūtni. stāvokļi (arteriālā hipertensija, cukura diabēts, sirds mazspēja, podagra utt.).
Lipīdu vielmaiņas traucējumu diētas korekciju pacientiem ar hiperholesterinēmiju vēlams papildināt ar holesterīna līmeni asinīs pazeminošu medikamentu lietošanu. Papildus holestiramīnam un nikotīnskābe, probukols, lipostabils, gemfibrozils, kuriem ir mērena hipoholesterinēmiska iedarbība, un īpaši lovastatīns, kas izjauc vienu no holesterīna sintēzes saitēm un, acīmredzot, palīdz palielināt šūnu receptoru skaitu zema blīvuma lipoproteīniem, ir sevi pierādījuši labi. Nepieciešamība pēc ilgstošas šādu zāļu lietošanas ārstus pamatoti satrauc par to lietošanas drošību. Savukārt koronārās aterosklerozes stabilizēšanās vai pat reversas attīstības iespēja ir saistīta ar ilgtspējīgu (vismaz 1 gadu) holesterīna līmeņa pazemināšanos asinīs līdz 5 mmol/l (200 mg/100 ml) vai mazāk. Tik ievērojams holesterīna satura samazinājums un tā stabilizēšana tik zemā līmenī ir visreālākā, ja tiek izmantotas lovastatīna vai ekstrakorporālās asins attīrīšanas metodes (hemosorbcija, imūnsorbcija), ko galvenokārt izmanto ģimenes hiperlipidēmijai.
Antianginālu zāļu lietošana ir neaizstājama sastāvdaļa kompleksa ārstēšana pacienti, kuriem bieži rodas stenokardijas vai tās ekvivalentu lēkmes. Izteikts antiangināls efekts ir raksturīgs nitrātiem, kas samazina koronārās artērijas tonusu stenozes vietā, novērš tās spazmu, paplašina kolaterales un samazina slodzi uz sirdi, samazinot venozo asiņu atteci sirdī un paplašinot perifērās arteriolas. .
Stenokardijas lēkmes atvieglošanai, kā arī profilakses nolūkos dažas minūtes pirms slodzes lieto sublingvālo nitroglicerīnu (1-2 tabletes pa 0,5 mg). Dažādi novērš uzbrukumus dažu stundu laikā zāļu formas ilgstošas darbības nitroglicerīns (sustak, nitrong, nitroglicerīna ziede, trinitrolongs plākšņu veidā uz smaganām utt.). Starp ilgstošas darbības nitrātiem izceļas nitrosorbīds, kam raksturīga visstabilākā koncentrācija asinīs un salīdzinoši lēna tolerances attīstība pret to. Lai novērstu tolerances veidošanos pret nitrātiem, ieteicams tos izrakstīt periodiski vai tikai paaugstinātas fiziskās aktivitātes, psihoemocionālā stresa vai slimības saasināšanās periodos. Miokarda skābekļa pieprasījuma samazināšanai tiek izmantoti β-adrenerģiskie blokatori, kas, samazinot adrenerģisko ietekmi uz sirdi, samazina sirdsdarbības ātrumu, sistolisko asinsspiedienu, sirds un asinsvadu sistēmas reakciju uz fizisko un psihoemocionālo stresu. Šādas atsevišķu šīs grupas zāļu īpašības, piemēram, kardioselektivitāte, membrānas stabilizējošās īpašības un to pašu adrenomimētiskās aktivitātes klātbūtne būtiski neietekmē antianginālo efektivitāti, taču tās jāņem vērā, izvēloties zāles pacientiem ar aritmiju, sirds mazspēju un vienlaicīga bronhu patoloģija. Izvēlētā β-adrenerģiskā blokatora devu izvēlas individuāli katram pacientam; ilgstošai uzturošai terapijai ērti ir ilgstošas darbības medikamenti (metoprolols, tenolols, lēnas darbības propranolols).Adrenerģiskie blokatori ir kontrindicēti sirds glikozīdu nekompensētas sastrēguma sirds mazspējas gadījumā, bronhiālā astma, smaga bradikardija (mazāk nekā 50 sirds sitieni minūtē), ar asinsspiedienu zem 100/60 mm Hg. Art. arteriāla hipotensija, slima sinusa sindroms, II-III pakāpes atrioventrikulārā blokāde. Ilgstoši lietojot beta blokatorus, var rasties aterogēnas izmaiņas asins lipīdu sastāvā. Ārstējot ar šīm zālēm, ārstam ir jābrīdina pacients par viņu pēkšņas atcelšanas draudiem, jo pastāv strauja IBS saasināšanās risks. Pacienti ar aritmiju, kuriem adrenerģiskie blokatori ir kontrindicēti. Var ordinēt amiodaronu (kordaronu), kam ir gan antiaritmiska, gan antiangināla iedarbība.
Kalcija antagonistus kā antianginālus līdzekļus izmanto visu I.b.s formu ārstēšanai. bet tie ir visefektīvākie angiospastiskās stenokardijas gadījumā. Katrai no visbiežāk lietotajām zālēm (nifedipīnam, verapamilam un diltiazemam) ir specifiska ietekme uz atsevišķām sirds funkcijām, kas tiek ņemta vērā, nosakot indikācijas to lietošanai. Nifedipīns (Corinfar) praktiski neietekmē sinusa mezglu un atrioventrikulāro vadīšanu, tam piemīt perifēro vazodilatatora īpašības, tas pazemina asinsspiedienu, tiek parakstīts pacientiem ar sirds mazspēju un ir labvēlīgs bradikardijas gadījumā (nedaudz palielina sirdsdarbības ātrumu). Verapamils inhibē sinusa mezgla darbību, atrioventrikulāro vadīšanu un kontraktilās funkcijas (var pasliktināt sirds mazspēju). Diltiazemam piemīt abu zāļu īpašības, taču tas mazāk inhibē sirds darbību nekā verapamils un samazina asinsspiedienu mazāk nekā nifedipīns.
Antianginālu zāļu kombinācijas dažādas grupas parakstītas saasināšanās un smagas stenokardijas gadījumā, kā arī, ja nepieciešams koriģēt vienu zāļu nelabvēlīgo ietekmi ar pretēju iedarbību citām zālēm. Tātad, piemēram Refleksā tahikardija, ko dažkārt izraisa nifedipīns un nitrāti, samazinās vai nenotiek, vienlaikus lietojot adrenerģiskos blokatorus. Slodzes stenokardijas gadījumā nitrāti ir “pirmās rindas” zāles, kurām pievieno adrenerģiskos blokatorus un/vai verapamilu vai diltiazemu, nifedipīnu.
Kopā ar antiangināliem līdzekļiem I.b.s. paasinājumu ārstēšanai un profilaksei. Efektu iedarbojas līdzekļi, kas nomāc funkcionālo aktivitāti un trombocītu agregāciju. No šiem līdzekļiem visbiežāk lietotā ir acetilsalicilskābe, kas noteiktā devā var radīt nelīdzsvarotību starp tromboksānu un prostaciklīnu par labu pēdējam, bloķējot prekursoru veidošanos tromboksāna A sintēzei. Efektu panāk, lietojot nelielas acetilsalicilskābes devas - ne vairāk kā 250 mg dienā. Ilgstoša ārstēšana ar šīm zālēm samazina miokarda infarktu skaitu pacientiem ar nestabilu stenokardiju un recidivējošu miokarda infarktu skaitu.
Koronārās sirds slimības ķirurģiskā ārstēšana, neskaitot tās komplikāciju ārstēšanu (pēcinfarkta sirds aneirismas izgriešana u.c.), galvenokārt sastāv no koronāro artēriju šuntēšanas operācijas. UZ ķirurģiskas metodes Iekļauts arī īpašs intravaskulāras rekonstruktīvās iejaukšanās veids - tiek izstrādāta perkutāna balonu angioplastika, lāzera un citas angioplastikas metodes. Šo metožu izmantošana kļuva iespējama, pateicoties plašai selektīvās koronārās angiogrāfijas izmantošanai diagnostikas un ārstēšanas praksē.
Koronāro artēriju šuntēšanas operācija (KAB) ir indicēta III un IV funkcionālās klases stenokardijas gadījumā, kas būtiski ierobežo pacienta motorisko aktivitāti, un saskaņā ar koronārās angiogrāfijas rezultātiem – kreisās koronārās artērijas galvenā stumbra stenozei (vairāk nekā 70%), trīs galveno artēriju proksimālo daļu stenoze, kreisās koronārās artērijas priekšējā interventrikulārā zara proksimālā stenoze. Citos viena trauka bojājuma gadījumos operācija nav indicēta, jo tas neuzlabo dzīves prognozi. Proksimālās stenozes gadījumā operācija ir iespējama tikai tad, ja artērijas distālā daļa zem sašaurināšanās vai oklūzijas vietas ir apmierinoši piepildīta ar kontrastvielu.
Koronāro artēriju šuntēšana tiek veikta mākslīgās asinsrites apstākļos ar apturētu sirdi. Tas sastāv no šunta novietošanas starp aortu un koronārās artērijas daļu zem sašaurināšanās vai oklūzijas vietas. Lielākas tiek izmantotas kā anastomozes. saphenous vēna operējamās personas gurni un (vai) iekšējās piena dziedzeru artērijas. Šuntus novieto, ja iespējams, uz visām skartajām lielajām artērijām, kas ir stenozētas par 50% vai vairāk. Jo pilnīgāka ir revaskularizācija, jo augstāks ir pacientu izdzīvošanas rādītājs un labāki operācijas ilgtermiņa funkcionālie rezultāti.
Perkutāna balonu angioplastika (artērijas balonu paplašināšana) viena koronārā asinsvada (izņemot kreisās koronārās artērijas stumbra) sašaurināšanai ir kļuvusi par alternatīvu KAŠ. To sāka lietot arī vairāku koronāro artēriju vairākām stenozēm un koronāro artēriju šuntēšanas stenozēm. Fluoroskopijas kontrolē stenozes zonā tiek ievietots īpašs katetrs ar balonu galā. Kad balons tiek piepūsts, uz kuģa sieniņām tiek radīts spiediens, kas izraisa aterosklerozes plāksnes saspiešanu, saplacināšanu un attiecīgi koronārās artērijas lūmena paplašināšanos; Tajā pašā laikā rodas kuģa intima plīsumi. Veiksmīga iejaukšanās uzlabo pacientu stāvokli; stenokardija bieži izzūd pilnībā. Objektīvi ārstēšanas efektu apliecina pacienta fiziskās slodzes tolerances uzlabošanās, pēc veloergometrijas un koronārās angiogrāfijas datiem, kas liecina par skartās artērijas caurlaidības atjaunošanos (2. att.). Galvenais risks, ko izraisa koronāro artēriju paplašināšanās ar balonu, ir saistīts ar asinsvada oklūziju un perforāciju, kas var būt nepieciešama steidzama operācija CABG Koronārās angioplastikas trūkums ir restenozes rašanās, kas izskaidrojama ar palielināta aktivitāte trombocīti, kas saskaras ar asinsvadu sieniņu, kas bojāta paplašināšanās laikā aplikuma zonā, un pēc tam trombu veidošanās.
I.b.s. ķirurģiska ārstēšana. nav radikāls, jo koronāro artēriju ateroskleroze turpina progresēt, iesaistot jaunus asinsvadu gultnes apgabalus un palielinot iepriekš skarto asinsvadu stenozi. Šis process notiek gan apietajās, gan neapietajās artērijās.
Prognoze. Sakarā ar progresīvo I.b.s. un dažādu sirds funkciju (kontraktilitāte, automātisms, vadītspēja) miokarda išēmijas, nekrozes un sklerozes epizožu laikā, pacientu darba spēju un pašas dzīves prognoze vienmēr ir nopietna. Zināmā mērā dzīvībai svarīgo prognozi nosaka ķīlis. veidlapa I.b.s. un tā smaguma pakāpe, kas skaidri izpaužas, piemēram. nāves varbūtības atšķirībās ar dažādu funkcionālo klašu stabilu stenokardiju un ar miokarda infarktu, un ar pēdējo arī par nekrozes fokusa atrašanās vietu un lielumu miokardā. No otras puses, pēkšņa nāve, malas, var notikt ar salīdzinoši zemu koronāro artēriju bojājuma pakāpi bez iepriekšējiem ķīļiem. koronārās mazspējas izpausmes, veido 60 līdz 80% no visiem letālajiem I.b.s. Lielākā daļa pacientu mirst no sirds kambaru fibrilācija, saistīta ar miokarda elektrisko nestabilitāti, ko izraisa akūti attīstoša išēmija.
Atsauces
1. Gasiļins V.S. un Sidorenko B.A. “Stenokardija”, M. 1987;
2. Koronārā sirds slimība” I.E. Gaļeņina, L. 1997;
3. Mazur N.A. "Pacientu ar koronāro sirds slimību pēkšņa nāve," M. 1985;
4. Petrovskis B.V. “Hroniskas išēmiskas sirds slimības ķirurģija”, M. 1978;
5. Shkhvatsabaya I.K. “Sirds išēmiskā slimība”, M. 1975.
Zināms jau sen. Bet tā tika identificēta kā neatkarīga nosoloģiska vienība 1959. gadā ar PVO lēmumu.
Koronārā sirds slimība – saskaņā ar PVO galīgo definīciju – ir akūts un hronisks sirds bojājums, ko izraisa miokarda asins piegādes samazināšanās vai pārtraukšana koronāro artēriju aterosklerozes procesa dēļ.
Tas ir, IHD ir išēmisks sirds bojājums koronārās aterosklerozes dēļ.
IHD ir viens no sirds išēmiskā bojājuma variantiem, ko izraisa dažādu slimību izraisīti koronāro artēriju bojājumi.
Ir 3 sirds išēmisko bojājumu grupas:
nejauši;
iedzimts;
sekundārais - dažādām slimībām.
1. Nejauši. Piemēri:
dinamīta sirds darbiniekiem, kuri ilgstoši ir bijuši saskarē ar nitroglicerīnu un ātri pārtrauca šo kontaktu; miokarda išēmija šajā gadījumā rodas koronāro artēriju funkcionālas sašaurināšanās rezultātā pēc nitroglicerīna darbības pārtraukšanas;
traumas - ar koronāro artēriju asinsizplūdumu un trombozes attīstību;
koronāro artēriju tromboze, ilgstoši lietojot kontracepcijas līdzekļus.
2. Iedzimta. Tos novēro dažādās sirds un asinsvadu malformācijās.
3. Sekundārā. Saistīts ar koronāro artēriju bojājumiem un to lūmena sašaurināšanos slimību dēļ - sifiliss, tuberkuloze, sepsi, reimatiskas slimības, ateroskleroze un citas slimības.
Šajā daudzajā sirds išēmisko bojājumu sarakstā īpaša vieta aizņem koronāro artēriju aterosklerozi. Koronāro artēriju ateroskleroze veido 90-95% no visiem išēmiskiem sirds bojājumiem. Tāpēc tā tika identificēta kā īpaša nosoloģiska forma - IHD.
IHD klasifikācijas ir ļoti daudzas. Bet, mūsuprāt, patoloģijas būtības izpratnei vispiemērotākā ir klasifikācija, kas balstīta uz klīnisko un morfoloģisko principu, izšķirot 5 slimības formas:
Stenokardija.
Starpformas.
Liels fokālais miokarda infarkts.
Akūta koronārā mazspēja (pēkšņa nāve).
Hroniska koronārā mazspēja (išēmiska kardiomiopātija, nesāpīga forma).
Statistika.
Vecums - 40-49 gadi - IHD skar līdz 10% iedzīvotāju.
Vecums - 50-59 gadi - 20%
Vecākiem par 60 gadiem koronāro artēriju slimība vienā vai otrā veidā tiek novērota gandrīz katram attīstīto valstu iedzīvotājam, jo koronārās artērijas šajā vecumā skar ateroskleroze gandrīz ikvienam.
IHD patoģenēzi un klīniskās un morfoloģiskās izpausmes nosaka 2 faktoru grupas:
sirds artēriju stāvoklis;
miokarda stāvoklis.
1. Sirds artēriju stāvoklis.
Šī faktoru grupa ir saistīta ar sirds asinsapgādes veidu un koronāro artēriju aterosklerozes procesa attīstības pakāpi.
Sirds asins piegādes veidi:
Pa kreisi - dominē kreisā koronārā artērija.
Pa labi - labā koronārā artērija dominē.
Vidēja - abas artērijas ir vienlīdz attīstītas.
Vidējā kreisā artērija - dominē kreisā artērija, bet labā artērija ir attīstītāka nekā vidējā versijā.
Vidējā labā artērija - dominē labā artērija, bet kreisā artērija ir attīstītāka nekā vidējā variantā.
Rezultātā kreisais veids ir 10%, labais veids ir 5%, bet vidējais veids ir 85%. Šie faktori nosaka nodrošinājuma cirkulācijas attīstības pakāpi, kad koronārās artērijas ir bojātas ar aterosklerozi.
Aterosklerozes koronāro artēriju bojājumu dinamiku nosaka procesa stadija un slimības attīstības gaita.
Procesa posmi sakrīt ar aterosklerozes stadijām. Šis:
prelipīdu stadija;
lipoidoze;
liposkleroze;
ateromatozes;
čūlas veidošanās;
aterokalcinoze.
Koronāro artēriju prelipīdu un lipoidozes stadijās slimības klīniskās izpausmes neparādās vai kļūst nozīmīgas ar pārmērīgu stresu. Liposklerozes stadijā pat vienas šķiedru plāksnes klātbūtnē var attīstīties smaga išēmija. Slimības klīniskās pazīmes pastiprinās turpmākajos koronāro artēriju aterosklerozes posmos.
Procesa virzība. Ateroskleroze sākas proksimālajās koronārajās artērijās un pēc tam izplatās uz distālajām daļām. Tas dabiski ietekmē kompensējošo procesu veidošanos, kas izpaužas nodrošinājuma aprites attīstībā. Aterosklerozei progresējot uz distālajām daļām, ievērojami samazinās nodrošinājumu attīstības iespējas.
Stenozes kritiskā robeža ir lūmena sašaurināšanās līdz 85%.
Slimības attīstībā vienlaikus pastāv divi procesi - stenoze un obligātās asinsrites attīstība, kas atspoguļo kompensācijas un adaptācijas procesus.
Šajā gadījumā veidojas 3 nodrošinājuma līmeņi:
Makroarteriālas - anastomozes starp labo un kreiso koronāro artēriju.
Mazās artērijas - anastomozes starp intramuskulārām artērijām.
Mikrocirkulācijas - anastomozes mikrocirkulācijas gultnes līmenī subendokarda slānī ar dzīslenes pinumu veidošanos.
Miokarda stāvoklis.
2) nepietiekama asins piegāde dažādās zonās: asins piegādes intensitāte ir visizteiktākā subepikarda zonā, vismazāk - subendokarda zonā, un intrakardiālā zona ir vidējā stāvoklī;
3) regulējošo sistēmu ietekme:
nervozs: centrālais nervu sistēma, simpātiskās un parasimpātiskās sistēmas;
endokrīnie dziedzeri: virsnieru dziedzeri, reproduktīvie un vairogdziedzeri;
asins sastāvs: humorālie faktori, skābekļa piesātinājuma pakāpe, koagulācijas sistēmas stāvoklis.
IHD patoģenēze ir sarežģīta. Bet galvenā patoģenētiskā saikne ir neatbilstība starp asins piegādes intensitāti un miokarda vajadzību pēc pārtikas, kas attīstās išēmijas laikā.
Išēmijas cēlonis: asins plūsmas pretestības palielināšanās koronāro artēriju lūmena sašaurināšanās un miokarda nepietiekamas asins piegādes dēļ, pārejot no zemākas funkcijas uz intensīvāku.
Parasti izmaiņas asins apgādē (koronārā rezerve) ir proporcijā 1:30 (atpūta: maksimālais pieaugums). Ar koronāro artēriju aterosklerozi koronārā rezerve samazinās vairākas reizes un var sasniegt ārkārtīgi zemas attiecības (1: 3, 4, 5).
Sirds išēmiskās slimības riska faktori.
Pamata:
lipoproteīnu metabolisma pārkāpums;
arteriālā hipertensija;
pārtikas veids;
psihoemocionāls;
alkoholisms;
motora režīms;
augstākais veids nervu darbība– cilvēki ar A tipu ir sliktākā situācijā; viņi izceļas ar pārmērīgu pašapziņu, tieksmi pēc vadības par katru cenu, atkarību, agresivitāti un dusmas;
profesija;
endokrīnās slimības, piemēram: diabēts.
Visbiežāk darbojas dažādu faktoru kombinācija.
Klīniskās un morfoloģiskās īpašības dažādas formas IHD.
1. stenokardija.
Klīnika: sirds sāpes īslaicīgu lēkmju veidā, kas kļūst biežākas fiziska un garīga stresa laikā.
Uzbrukuma iespējas:
tipisks;
netipiski.
Netipiski:
grēmas formā;
lēkmes apgrūtināta elpošana;
sāpes starplāpstiņu zonā.
Stenokardijas patoģenēzi var definēt kā atgriezenisku koronāro mazspēju un mērenu hipoksiju. Tie attīstās, jo nespēj normāli apgādāt miokardu ar asinīm aterosklerozes bojātās koronārās artērijas darbības izmaiņu dēļ.
Koronārās mazspējas dinamika.
Sākotnējais posms. Uzbrukumi ir reti un notiek ar ievērojamu pārslodzi.
Izteiktu izpausmju stadija. Krampji normālas slodzes laikā.
Smaga stenokardija. Uzbrukumu rašanās fiziskās atpūtas stāvoklī. Stenokardija miera stāvoklī.
Stenokardijas patomorfoloģiju raksturo kā atgriezenisku miokarda un mikrovaskulāro bojājumu. Eksperiments parādīja, ka pēc īslaicīgas išēmijas stromā tiek novēroti:
pārpilnība;
asiņošanas zonas;
endotēlija distrofija.
miokardiocītos:
pinocitoze;
mitohondriju pietūkums;
glikogēna samazināšana;
lipīdu izskats;
miofibrilu kontraktūra un to primārā klupiena sadalīšanās.
Pēc išēmijas un vienlaikus hipoksijas likvidēšanas parasti notiek pilnīga atveseļošanās. Dažreiz smagu uzbrukumu laikā var rasties atsevišķu muskuļu šūnu nāve.
Sāpju patoģenēze stenokardijas gadījumā acīmredzami ir saistīta ar mediatoriem, kas uzkrājas, kad tiek bojāti kardiomiocīti.
2. IHD STARPFORMA.
Ir 3 formas:
fokusa distrofija;
neliels fokusa miokarda infarkts;
pirmsinfarkta sindroms.
Klīnikai raksturīgi smagi un ilgstoši stenokardijas lēkmes.
Patoģenēze: smaga hipoksija.
Patomorfoloģija:
fokusa vai plaši izplatīta miokardiocītu distrofija;
neliels fokālais miokarda infarkts.
pilnīga atveseļošanās;
maza fokusa kardioskleroze;
pirmsinfarkta stāvoklis ar pāreju uz liela fokusa miokarda infarktu.
3. LIELS FOKĀLS INFRAKTS. MIOKARDIJA.
Šī ir galvenā IHD forma. Bez aktīvas ārstēšanas 40% gadījumu tas beidzas ar pacienta nāvi viena mēneša laikā.
tipisks – 95%;
netipiski – 5%.
Raksturīgi: intensīvas sāpes no 30 minūtēm līdz dienai, ko neatbrīvo nitroglicerīns sirds rajonā ar raksturīgu apstarošanu.
Netipiski – 3 iespējas:
astmatisks;
gastralģiskas (sāpes kuņģī);
smadzeņu (krampji, ģībonis).
Liela fokāla miokarda infarkta klasifikācija.
Principi:
lokalizācija;
miokarda bojājuma dziļums;
plūsmas raksturs.
1. Lokalizācija:
99% - kreisais kambara, 1% - labais kambara.
Kreisais kambara:
posterolateral;
5anterolateral;
priekšējā-aizmugurējā.
priekšpuse;
2. Pamatojoties uz muskuļu sienas bojājuma dziļumu, izšķir 4 miokarda infarkta veidus:
transmurāls;
intramurāls;
subepikarda;
subendokardiāls.
3. Pēc kursa rakstura ir 6 miokarda infarkta varianti:
tipisks;
netipisks;
atkārtojas;
atkārtots;
ieilgušas;
Areaktīvs.
1) TIPISKS miokarda infarkts.
Posmi - 4:
pirmsnekrotisks;
nekrotisks;
organizācijas;
izmaiņas pēc infarkta;
Donekrotiskā stadija.
Ilgums - pirmās 5 stundas pēc ilgstošas išēmijas (30-60 minūtes vai vairāk).
Patomorfoloģija.
Makroskopisks attēls:
nevienmērīga miokarda pārpilnība;
nav redzamu sirdslēkmes pazīmju.
Mikroskopisks attēls:
mikrocirkulācijas traucējumi;
glikogēna izzušana un krusteniskās svītras miokardiocītos;
miofibrilu bojājumi (kontraktūra, primāra sašķelšanās, intracelulāra citolīze).
Elektronu mikroskopiskais attēls:
organellu izmaiņu polimorfisms;
mitohondriju bojājumi (daļēja, mērena un visbeidzot pilnīga iznīcināšana);
kodola un lizosomu aparāta bojājumi.
Histoķīmiskie pētījumi atklāj šādas izmaiņas kardiomiocītos:
fermentu trūkums;
neitrālu polisaharīdu uzkrāšanās;
nukleīnskābju un glikogēna samazināšana;
lipīdu izskats.
Nekrotiskā stadija.
Ilgums – līdz 5 dienām.
Patomorfoloģija
Makroskopisks attēls: svītru izzušana, homogenizācija, sirdslēkmei raksturīgi tumši sarkani un balti perēkļi.
Mikroskopiskā aina: infarkta zonā ir raksturīga muskuļu šķiedru nekroze, tūska, plazmorāģija, asinsizplūdumi, neitrofilu, makrofāgu uzkrāšanās, iekaisuma šūnu un fibroblastu robežzonas veidošanās. Ārpus infarkta zonas izmaiņas ir tādas pašas kā pirmsnekrotiskā stadijā + kardiomiocītu kompensējošā hipertrofija.
Organizācijas posms.
Ilgums: 3-45 dienas.
Patomofoloģija:
nekrotisko masu proteolīze
nekrotisko masu rezorbcija un to rezorbcija ar makrofāgiem
nekrozes fokusa aizstāšana ar saistaudiem
rupjas kolagēna rētas veidošanās pēc 1,5 – 2 mēnešiem. no slimības sākuma smalki tīklveida kardioskleroze ārpus infarkta zonas.
Pēcinfarkta izmaiņu stadija.
Ilgums – nenoteikts laiks.
Procesi:
rētas aizstāšana ar taukaudiem;
muskuļu šķiedru reģeneratīvā hipertrofija.
2. ATIPISKS miokarda infarkts.
Pazīmes: posmu pārkāpums, klīniskā atipija, patomorfoloģija, neparasta patoģenēze.
Klīnika - nesāpīga forma.
Vecums - vecāki cilvēki.
Patoģenēze – lēna hipoksija uz koronāro artēriju stenozes aterosklerozes fona.
Patomorfoloģija:
visbiežāk transmurāls infarkts;
nav skaidra zonējuma;
nekrozes un bojājumu perēkļu maiņa ar organizācijas zonām.
3. ATKĀRTOTS infarkts.
To raksturo procesa saasināšanās ar svaigu nekrozes perēkļu parādīšanos gar infarkta zonas malu līdz 2 mēnešiem.
4. ATKĀRTOTA sirdslēkme.
To raksturo svaigu nekrozes perēkļu parādīšanās infarkta zonā.
5. ILGSTS infarkts.
To raksturo organizatorisko procesu palēnināšanās, kas ilgst vairāk nekā 2,5 mēnešus. Patomorfoloģija izpaužas ar rētaudi, hialinozi, mirušo muskuļu šķiedru salām bez autolīzes pazīmēm un aizstāšanu ar saistaudiem.
6. AREAKTĪVAIS infarkts.
Raksturīga ar iekaisuma reakcijas un organizatorisko procesu pavājināšanos. Tas attīstās vecumdienās uz koronāro artēriju smagas stenozes aterosklerozes fona.
Miokarda infarkta komplikācijas.
Akūts periods. 8 grupas:
Sirdskaite.
Ritma traucējumi.
Ventrikulāra fibrilācija.
Kardiogēns šoks.
Sienas plīsums.
Akūta sirds aneirisma.
Trombembolija.
Kuņģa-zarnu trakta un urīnceļu sistēmas patoloģija.
Sirdskaite. Manifestācijas: tahikardija, cianoze, elpas trūkums. Tā var būt mērena, smaga, bronhiālās astmas un plaušu tūskas veidā. Patoģenēze ir miokarda kontraktilās funkcijas pārkāpums.
Ritma traucējumi. Patoģenēze – impulsu vadīšanas traucējumi. Iemesli ir smagas vielmaiņas izmaiņas un deģeneratīvi procesi miokardiocītos, kā arī vadīšanas ceļos.
Ventrikulāra fibrilācija. Patoģenēze - impulsu apļveida un virpuļveida kustības. Patomorfoloģija - vairāki atgriezeniski, kontraktūras bojājumi muskuļu šķiedrām zem endokarda un epikarda.
Kardiogēns šoks. Klīnika - sabrukums, straujš asinsspiediena pazemināšanās. Pazīmes: bālums, cianoze, auksti sviedri, samaņas zudums, akūta nieru mazspēja. Patomorfoloģija - traucēta mikrocirkulācija un atgriezenisks kardiomiocītu bojājums ārpus infarkta zonas.
Ventrikulāras sienas plīsums. Sekas ir sirds tamponāde un pacienta nāve akūtas sirds un asinsvadu mazspējas simptomu dēļ.
Akūta sirds aneirisma. Nolietotās kambara sienas izspiedums infarkta zonā miomalācijas rezultātā.
Trombembolija. Avots ir asins recekļi sirdslēkmes zonā. Tiek ietekmēti dažādi orgāni sistēmiskās asinsrites zonā.
Kuņģa-zarnu trakta un urīnceļu sistēmas patoloģija. Veidi:
kuņģa un zarnu parēze;
2 čūlas kuņģa un zarnu gļotādā;
pankreatīts;
urīna aizture urīnpūšļa parēzes dēļ.
Pēcinfarkta periods.
Komplikācijas:
alerģija;
hroniska sirds mazspēja.
perikardīts;
pneimonija;
4. AKŪTA KORONĀRĀ IZMAIŅA (pēkšņa nāve).
Klīniskā aina ir smags pirmsinfarkta stāvoklis. Pēkšņa nāve kambaru fibrilācijas dēļ. Bieži vien šīs ir pirmās IHD izpausmes.
Patomorfoloģija - koronāro artēriju stenozējoša ateroskleroze + muskuļu šķiedru grupu kontraktūras bojājumi dažādās kreisā kambara sienas zonās.
5. HRONISKĀ KORONĀRĀ NEPIECIEŠAMĪBA (aterosklerozes kardioskleroze, kardiomiopātija).
Visizplatītākā IHD forma.
Kurss ir ilgstošs bez katastrofām liela fokusa miokarda infarkta veidā. Visbiežāk nesāpīga forma.
Patomorfoloģija - difūzā mazā fokālā kardioskleroze
Klīniskā aina ir pakāpeniska, ilgstoša sirds mazspējas palielināšanās.
Patoģenēze – mērena hroniska hipoksija.
Secinājums.
IHD ir izplatīta un smaga patoloģija. Bet ar vispāratzītu profilaksi un ārstēšanu ar šo slimību var veiksmīgi cīnīties. Cīņas principi ir diēta, dzīvesveida normalizēšana, riska faktoru izslēgšana, lipoproteīnu metabolisma korekcija.
Makro un mikro sagatavošanās lekcijai
65. attēls - Miokarda infarkts.

66. attēls - Miokarda infarkts.

67. attēls - kreisā kambara sienas plīsums (sirds tamponāde).

68. attēls - akūta koronārā mazspēja.
IHD– akūta vai hroniska miokarda disfunkcija, ko izraisa relatīvs vai absolūts arteriālo asiņu piegādes samazinājums miokardam, kas visbiežāk saistīts ar patoloģisku procesu koronāro artēriju (KA) sistēmā.
IHD etioloģija:
1. Koronārās artērijas ateroskleroze - visbiežāk tiek skarts kreisās koronārās artērijas priekšējais lejupejošais zars, retāk kreisās koronārās artērijas cirkumfleksais zars un labā koronārā artērija.
2. Iedzimtas koronārās artērijas anomālijas (cirkumfleksās artērijas izcelsme no labās koronārās sinusa vai labās koronārās artērijas utt.)
3. Koronārās artērijas sadalīšana (spontāna vai aortas aneirismas sadalīšanas dēļ)
4. Koronāro artēriju iekaisuma bojājumi (ar sistēmisku vaskulītu)
5. Sifilīts aortīts ar procesa izplatīšanos uz koronāro artēriju
6. Koronārās artērijas radiācijas fibroze (pēc videnes apstarošanas limfogranulomatozes un citu audzēju gadījumā)
7. Koronārās artērijas embolija (biežāk ar IE, MA, retāk ar reimatiskiem defektiem)
Pašlaik IHD tiek uzskatīta par miokarda išēmiju, ko izraisa tikai aterosklerozes process koronārajā artērijā.
Koronārās sirds slimības riska faktori:
A. Modificēts: 1) cigarešu smēķēšana 2) arteriāla hipertensija 3) cukura diabēts 4) zems ABL holesterīna līmenis, augsts ZBL holesterīna līmenis, kopējais holesterīns virs 6,5 mmol/l 5) aptaukošanās
b. Nepārveidojams: 1) vecums: 55 gadi un vecāki vīriešiem, 65 gadi un vecāki sievietēm 2) vīriešu dzimums 3) IHD ģimenes anamnēze
Arī izceļas pamata(vecums virs 65 gadiem sievietēm un virs 55 gadiem vīriešiem, smēķēšana, kopējais holesterīns > 6,5 mmol/l, koronāro artēriju slimība ģimenes anamnēzē) un cits(zems ABL holesterīna līmenis, augsts ZBL holesterīna līmenis, traucēta glikozes tolerance, aptaukošanās, mikroalbuminūrija diabēta gadījumā, mazkustīgs dzīvesveids, paaugstināts fibrinogēna līmenis) koronāro artēriju slimības riska faktori.
IHD patoģenēze.
Parasti pastāv skaidra atbilstība starp skābekļa piegādi kardiomiocītiem un nepieciešamību pēc tā, nodrošinot normālu vielmaiņu un sirds šūnu darbību. Koronāro aterosklerozi izraisa:
A) koronāro artēriju mehāniska obstrukcija ar samazinātu šūnu perfūziju
b) koronārās artērijas dinamiska obstrukcija - koronārā spazma- sakarā ar aterosklerozes koronāro artēriju paaugstinātu reaktivitāti pret vazokonstriktoru (kateholamīni, serotonīns, endotelīns, tromboksāns) darbību un samazinātu reaktivitāti pret vazodilatatoru (endotēlija relaksējošais faktors, prostaciklīns) darbību.
V) mikrocirkulācijas traucējumi– sakarā ar tendenci veidot nestabilus trombocītu agregātus skartajās koronārajās artērijās vairāku bioloģiski aktīvo vielu (tromboksāna A 2 utt.) izdalīšanās laikā, kas bieži vien spontāni sadalās.
G) koronārā tromboze– aterosklerozes plāksnes bojājumu zonā uz trombogēnā subendotēlija veidojas asins recekļi, kas pastiprina išēmiju
Viss iepriekš minētais izraisa nelīdzsvarotību starp miokarda vajadzību pēc skābekļa un tā piegādi, traucētu sirds perfūziju un išēmijas attīstību ar sekojošām klīniskām izpausmēm stenokardijas sāpju, MI utt.
IHD klasifikācija:
1. Pēkšņa koronārā nāve (primārais asinsrites apstāšanās).
2. Stenokardija:
a) stenokardija: 1) pirmo reizi (līdz 1 mēnesim); 2) stabils (vairāk nekā 1 mēnesis); 3) progresīvs
b) spontāna (vazospastiska, īpaša, varianta, Princmetāla stenokardija)
3. Miokarda infarkts: a) ar Q-viļņu (liels fokālais - transmurāls un netransmurāls) b) bez Q-viļņa (mazs fokālais)
4. Pēcinfarkta kardioskleroze (2 mēnešus pēc MI)
5. Sirds ritma traucējumi
6. Sirds mazspēja
7. Nesāpīga (“klusā”) išēmija
8. Mikrovaskulāra (distālā) išēmiskā sirds slimība
9. Jauni išēmiski sindromi (miokarda apdullināšana, miokarda hibernācija, išēmiska miokarda sagatavošana)
Dažas IHD klīniskās formas - jauna stenokardija, progresējoša stenokardija, miera stenokardija un agrīna pēcinfarkta stenokardija (pirmās 14 dienas pēc MI) - ir formas nestabila stenokardija.
Ārstēšana– skatīt 20. jautājumu.
20. Koronārā sirds slimība: stenokardija. Etioloģija, patoģenēze, klīniskie varianti, diferenciāldiagnoze. Pacientu vadības taktika, ārstēšanas principi. Medicīniskā un sociālā pārbaude. Rehabilitācija.
Stenokardija- slimība, ko raksturo sāpju lēkmes krūtīs, kas rodas, reaģējot uz miokarda skābekļa metabolisma pieprasījuma palielināšanos fiziska vai emocionāla stresa dēļ; Šis sindroma jēdziens, klīniski raksturo vairākas pazīmes:
1) sāpju rašanās apstākļi - fiziska slodze vai emocionāls stress, auksta gaisa iedarbība
2) sāpju raksturs – spiežot, dedzinot, spiežot
3) sāpju lokalizācija - retrosternālais reģions vai precordial reģions pa kreisi no krūšu kaula
4) sāpju apstarošana - kreisajā rokā gar elkoņa kaula malu līdz mazajam pirkstiņam, kreisajā lāpstiņā, apakšžoklī
5) sāpju ilgums – 2-3 minūtes, bet ne vairāk kā 10-15 minūtes; izzūd pēc fiziskās aktivitātes samazināšanas vai pārtraukšanas
6) sāpes ātri un pilnībā izzūd pēc nitroglicerīna lietošanas pēc 3-5, bet ne vairāk kā 10 minūtes
Galvenās stenokardijas klīniskās formas un to īpašības.
1. Stenokardija:
A) pirmo reizi parādījās– slimības ilgums līdz 1 mēnesim; kam raksturīga polimorfa gaita - tā var regresēt, pāraugt stabilā stenokardijā vai iegūt progresējošu gaitu, tāpēc nepieciešama intensīva uzraudzība un ārstēšana
b) stabils(norādot funkcionālo klasi) – slimības ilgums ir ilgāks par 1 mēnesi; ko raksturo stereotipiskas sāpes, reaģējot uz parasto slodzi šim pacientam
V) progresīvs– veidojas biežāk uz stabilitātes fona; ko raksturo stenokardijas lēkmju biežuma, ilguma un intensitātes palielināšanās ar krasu pacienta fiziskās aktivitātes tolerances samazināšanos, ar lokalizācijas zonas paplašināšanos, sāpju apstarošanas ceļiem un nitroglicerīna lietošanas ietekmes pavājināšanos.
2. Spontāna (īpaša) stenokardija– ko raksturo stenokardijas sāpju lēkmes, kas rodas bez redzamas saistības ar faktoriem, kas palielina miokarda skābekļa patēriņu; vairumam pacientu sāpju sindroms attīstās stingri noteiktā diennakts laikā (parasti naktī vai pēc pamošanās), strukturāli sastāv no 3-5 sāpīgu epizožu ķēdes, kas mijas ar nesāpīgām pauzēm.
3. Nesāpīga (“klusā”) stenokardija– tiek diagnosticēts, kad EKG laikā tiek konstatētas skaidras išēmiskas izmaiņas ikdienas uzraudzība vai veicot stresa testus, kas neuzrāda nekādas pazīmes klīniskās pazīmes
4. Mikrovaskulāra stenokardija (X sindroms)– raksturīga tipiska stenokardijas klīniskā aina, EKG tiek konstatēta išēmija stresa vai farmakoloģisko izmeklējumu laikā ar nemainītām koronārajām artērijām saskaņā ar koronāro angiogrāfiju; izraisa defektīva no endotēlija atkarīga mazo miokarda arteriolu vazodilatācija, kas izraisa koronārās asins plūsmas rezerves samazināšanos un miokarda išēmiju
Stenokardijas diagnostika.
1. Anamnēzes dati (sāpju rašanās nosacījumi) un raksturīga klīniskā aina.
2. EKG: miera stāvoklī un lēkmes laikā, Holtera monitorings - specifisks stenokardijai ir ST segmenta izmežģījums 1 mm uz leju (subendokardiāla išēmija) vai uz augšu (transmurālā išēmija) no izolīna, visbiežāk reģistrē lēkmes brīdī.
3. Stresa testi: VEP, skrejceliņš, transezofageālā sirds stimulācija (reaģējot uz sirdsdarbības ātruma palielināšanos, EKG rodas išēmisks bojājums), farmakoloģiskie testi ar dobutamīnu un izadrīnu (izraisa miokarda skābekļa pieprasījuma palielināšanos), dipiridamols un adenozīns ( izraisīt zagšanas sindromu, paplašinot galvenokārt neskartus asinsvadus) - ļauj noteikt miokarda išēmiju, kas miera stāvoklī nav nosakāma, un noteikt koronārās mazspējas smagumu.
Miokarda išēmijas pazīmes stresa testu laikā:
a) stenokardijas lēkmes rašanās
b) horizontāla vai slīpa tipa ST segmenta pazemināšanās vai paaugstināšanās par 1 mm vai vairāk vismaz 0,8 sekundes no punkta j
c) R viļņa amplitūdas palielināšanās kombinācijā ar ST segmenta depresiju
4. Miokarda radionuklīdu scincigrāfija ar 201 Tl (absorbē normāls miokards proporcionāli koronārajai perfūzijai) vai 99 m Tc (selektīvi uzkrājas miokarda nekrozes zonās)
5. Echo-CG (ieskaitot stresa Echo-CG, Echo-CG ar farmakoloģiskiem testiem) – ļauj novērtēt lokālu un lielāku miokarda kontraktilitāti (traucēta lokālā kontraktilitāte atbilst išēmijas fokusam)
6. Koronārā angiogrāfija ir "zelta standarts" koronāro artēriju slimības diagnosticēšanai; veic biežāk, lai atrisinātu iespējamības jautājumu ķirurģiska ārstēšana
7. Elektrokardiotopogrāfija – 60 novadījumu EKG kartēšana
8. Pozitronu emisijas tomogrāfija - sniedz informāciju par koronāro asins plūsmu un miokarda dzīvotspēju
9. Obligātie laboratoriskie izmeklējumi: CBC, BAM, cukura līmenis asinīs, BAC (lipīdu profils, elektrolīti, sirds specifiskie enzīmi: CPK, AST, LDH, mioglobīns, troponīns T), koagulogramma.
Stenokardijas funkcionālās klasesļauj novērtēt koronāro artēriju slimību pacientu funkcionālo stāvokli un toleranci pret fiziskām aktivitātēm.
Mirstība no sirds un asinsvadu slimības(CVD) Krievijā joprojām ir augsts gan vispārējo, gan standartizēto rādītāju ziņā. Sirds un asinsvadu mirstība lielā mērā ir saistīta ar koronāro sirds slimību (KSS).
Pēc Rosstat datiem, 2011.gadā valstī ar koronāro artēriju slimības diagnozi tika novēroti 7 miljoni 411 tūkstoši pacientu, un pirmo reizi gada laikā šī diagnoze tika noteikta 738 tūkstošiem pacientu. Tajā pašā gadā IHD diagnoze kā nāves cēlonis norādīta 568 tūkstošos gadījumu, kas ir 397,4 uz 100 tūkstošiem iedzīvotāju. Mūsu valstī koronāro artēriju slimība starp visiem KVS ir biežākais iemesls, kāpēc pieaugušie apmeklē medicīnas iestādes (28% gadījumu).
Tomēr faktiskais pacientu skaits ar koronāro artēriju slimību ir ievērojami lielāks. Saskaņā ar Krievijas akūtu koronāro sindromu (AKS) reģistru gandrīz pusei pacientu ar akūtu koronāro mazspēju pirmā IHD izpausme ir miokarda infarkts (MI). Līdz ar to var pieņemt, ka tikai 40-50% no visiem pacientiem ar koronāro sirds slimību zina, ka viņiem ir slimība un saņem atbilstošu ārstēšanu, savukārt 50-60% gadījumu slimība paliek neatpazīta.
Ar vecumu palielinās koronāro artēriju slimības un tās izplatītākās formas stenokardijas izplatība un izlīdzinās sastopamības atšķirības starp dzimumiem.
Stabilas stenokardijas pacientu ikgadējais mirstības rādītājs ir gandrīz 2%, un vēl 2-3% pacientu katru gadu piedzīvo neletālu miokarda infarktu. Pacienti, kuriem diagnosticēta stabila stenokardija, mirst no koronāro artēriju slimības 2 reizes biežāk nekā cilvēki bez šīs slimības. Vīrieši ar stenokardiju dzīvo vidēji par 8 gadiem mazāk nekā tie, kuriem nav šīs slimības.
Koronārā sirds slimība ir miokarda bojājums, ko izraisa traucēta asins plūsma caur koronārajām artērijām. Koronāro artēriju bojājumi var būt organiski (neatgriezeniski) vai funkcionāli (pārejoši). Galvenais koronāro artēriju organisko bojājumu cēlonis ir stenozējoša ateroskleroze. Koronāro artēriju funkcionālo bojājumu faktori ir spazmas, pārejoša trombocītu agregācija un intravaskulāra tromboze.
Jēdziens “IHS” ietver akūtu pārejošu un hronisku patoloģiski apstākļi. Vairumā gadījumu galvenie IHD attīstības iemesli ir stabila anatomiskā aterosklerotiskā un/vai funkcionālā epikarda asinsvadu stenoze un/vai mikrocirkulācija. Citi IHD cēloņi (< 5 % случаев) являются: врожденные аномалии отхождения коронарных артерий, бактериальный эндокардит, передозировка сосудосуживающих препаратов и некоторых narkotiskās vielas, koronāro artēriju difūzā stenoze transplantētā sirdī u.c.
Galvenie modificējamie koronāro artēriju slimības riska faktori ir hiperholesterinēmija; arteriālā hipertensija; cukura diabēts; smēķēšana; zema fiziskā aktivitāte; aptaukošanās.
Nemodificējami KSS riska faktori ir vīriešu dzimums; vecums; ģimenes anamnēzē sirds un asinsvadu slimības.
No koronāro artēriju slimības patoģenēzes viedokļa miokarda išēmija rodas, ja miokarda nepieciešamība pēc skābekļa pārsniedz tā piegādes spēju pa koronārajām artērijām. Galvenie išēmijas mehānismi ir: samazināta spēja palielināt koronāro asins plūsmu, palielinoties miokarda vielmaiņas vajadzībām (samazināta koronārā rezerve); primārā koronārās asinsrites samazināšanās.
Miokarda skābekļa patēriņu nosaka trīs galvenie faktori: kreisā kambara (LV) sienas spriegums; sirdsdarbība; miokarda kontraktilitāte. Jo augstāka ir katra no šiem rādītājiem vērtība, jo lielāks ir miokarda skābekļa patēriņš.
Koronārās asins plūsmas apjoms ir atkarīgs no trim galvenajiem faktoriem: koronāro artēriju pretestība; sirdsdarbība; perfūzijas spiediens (atšķirība starp diastolisko spiedienu aortā un diastolisko spiedienu LV).
Koronārā sirds slimība var rasties hroniskas išēmiskas sirds slimības (KSS) un akūta koronārā sindroma (AKS) formā.
Hroniska IHD forma var būt stenokardijas formā, kuras cēloņi var būt epikarda artēriju stenoze, mazo asinsvadu disfunkcija, vazokonstrikcija dinamiskas stenozes zonā vai stenokardija miera stāvoklī, kuras cēloņi var būt vazospazmas (lokālas vai difūzas) epikarda artēriju stenozes zonā, difūzas epikarda asinsvadu spazmas, mazo asinsvadu spazmas un iepriekš minēto iemeslu kombinācija vai asimptomātiskas miokarda išēmijas klīnisku vai instrumentālu pazīmju trūkuma dēļ un/vai LV disfunkcija.
Hroniska išēmiska sirds slimība var būt salīdzinoši labdabīga daudzu gadu garumā. Pastāv stabilas simptomātiskas vai asimptomātiskas fāzes, kuras var pārtraukt AKS attīstība. Pakāpeniska koronāro artēriju aterosklerozes un sirds mazspējas progresēšana izraisa pacientu funkcionālās aktivitātes samazināšanos un dažos gadījumos. akūtas komplikācijas(nestabila stenokardija, MI), kas var būt letāla (pēkšņa sirds nāve).
Mūsdienu IHD klasifikācija ietver
- pēkšņa kardiāla nāve (nāve liecinieku klātbūtnē, kas iestājas uzreiz vai 6 stundu laikā pēc sirdslēkmes sākuma);
- stenokardija: stenokardija, kas pirmo reizi ietver slodzes stenokardiju (slimības ilgums līdz 1 mēnesim no sākuma brīža); stabila slodzes stenokardija, kas norāda uz IIV funkcionālo klasi (slimības ilgums pārsniedz 1 mēnesi); progresējoša slodzes stenokardija (palielināts lēkmju biežums, smagums un ilgums, reaģējot uz pacienta normālu slodzi, samazināta nitroglicerīna efektivitāte; dažreiz izmaiņas EKG); spontāna stenokardija: vazospastiska, īpaša, variants, Prinzmetāls (lēkmes rodas miera stāvoklī, ir grūti reaģēt uz nitroglicerīnu, var kombinēt ar slodzes stenokardiju);
- miokarda infarkts, kurā izšķir divas formas: ar Q viļņu (liels fokāls, transmurāls) un bez Q viļņa (mazs fokāls, intramurāls, subendokardiāls);
- asinsrites mazspēja (išēmiska kardiopātija);
- sirds ritma traucējumi;
- nesāpīga (“klusa”) išēmija;
- mikrovaskulāra (distālā) išēmiskā sirds slimība;
- jauni išēmiski sindromi (miokarda “apdullināšana”, miokarda “ziemošanas miegs”).
Tipiskas (neapšaubāmas) stenokardijas pazīme ir sāpes krūšu kaulā, kas, iespējams, izstaro kreiso roku, muguru vai apakšžokli, ilgst 2-5 minūtes, rodas smaga emocionāla stresa vai fiziskas slodzes laikā; ātri izzūd pēc fiziskās aktivitātes pārtraukšanas vai pēc nitroglicerīna lietošanas. Sāpju ekvivalenti ir elpas trūkums, “smaguma”, “dedzināšanas” sajūta. Ir netipiski apstarošanas veidi (uz epigastrālo reģionu, uz lāpstiņu, uz krūškurvja labo pusi).
Galvenā piepūles stenokardijas pazīme ir skaidra simptomu rašanās atkarība no fiziskās aktivitātes. Stenokardijas ekvivalenti var būt elpas trūkums (pat nosmakšana), “karstuma” sajūta krūšu kaulā un aritmijas lēkmes fiziskās aktivitātes laikā. Fizisko aktivitāšu ekvivalents var būt asinsspiediena krīzes paaugstināšanās, palielinoties slodzei uz miokardu, kā arī liela maltīte.
Aptaujas laikā atkarībā no pieļaujamās fiziskās aktivitātes tiek izdalītas 4 stenokardijas funkcionālās klases (saskaņā ar Kanādas Kardiologu biedrības klasifikāciju):
- FC I (“latentā” stenokardija) ietver pacientus, kuriem lēkmes rodas tikai ārkārtēja stresa apstākļos;
- FC II ietver pacientus, kuriem stenokardijas lēkmes rodas normālas fiziskās slodzes laikā: ātra staigāšana, kāpšana kalnā, pa kāpnēm (vairāk nekā 1-2 lidojumi), pēc smagas maltītes, smags stress;
- III FC stenokardijas lēkmes krasi ierobežo fiziskās aktivitātes, tās rodas ar nelielu piepūli: ejot ar vidējo tempu, kas mazāks par 500 m, kāpjot pa 1-2 kāpnēm, reizēm lēkmes rodas miera stāvoklī;
- FC IV pacienti nespēj veikt nekādu, pat minimālu slodzi, stenokardijas rašanās dēļ lēkmes rodas miera stāvoklī, bieži anamnēzē ir MI un sirds mazspēja.
Ievērojama daļa miokarda išēmijas epizožu rodas, ja nav stenokardijas vai tās ekvivalentu simptomu, līdz attīstās kluss MI.
Hroniskas išēmiskas sirds slimības ietvaros ir 2 veidu klusā miokarda išēmija (SPMI):
- I tips ir pilnīgi nesāpīga miokarda išēmija;
- II tips ir nesāpīgu un sāpīgu miokarda išēmijas epizožu kombinācija.
BBMI epizodes parasti tiek atklātas slodzes testēšanas un 24 stundu EKG uzraudzības laikā. Pilnīgi klusa miokarda išēmija tiek atklāta aptuveni 18-25% cilvēku ar pierādītu koronāro artēriju aterosklerozi. Ar vienlaicīgu cukura diabētu I un II tipa BBIM iespējamība ir lielāka.
Hroniskas išēmiskas sirds slimības diagnoze balstās uz aptauju un slimības vēsturi; fiziskā pārbaude; instrumentālās studijas; laboratorijas pētījumi. Pirms jebkādas pārbaudes veikšanas ir jānovērtē pacienta vispārējais veselības stāvoklis, blakusslimības un dzīves kvalitāte (QoL).
Vairumā gadījumu hroniskas išēmiskas sirds slimības fiziskā pārbaude nav īpaši specifiska. Ir nepieciešams identificēt koronāro artēriju slimības riska faktoru pazīmes un komplikāciju simptomus. Sirds mazspējas simptomi (elpas trūkums, sēkšana plaušās, kardiomegālija, auļošanas ritms, jūga vēnu pietūkums, hepatomegālija, kāju pietūkums), perifēro artēriju ateroskleroze (intermitējoša klucikācija, artēriju pulsācijas pavājināšanās un muskuļu atrofija) ir svarīga diagnostiska un nelabvēlīga prognostiska nozīme. apakšējās ekstremitātes), arteriāla hipertensija, aritmija, troksnis pār miega artērijām.
Turklāt jums vajadzētu pievērst uzmanību liekajam ķermeņa svaram un ārējie simptomi anēmija, cukura diabēts (skrāpējumi, sausa un ļengana āda, samazināta ādas jutība, ādas trofikas traucējumi). Pacientiem ar ģimenes hiperholesterinēmijas formām rūpīga izmeklēšana var atklāt ksantomas uz rokām, elkoņiem, sēžamvietām, ceļiem un cīpslām, kā arī ksanthelasmas uz plakstiņiem.
Noteikti aprēķiniet ķermeņa masas indeksu, vidukļa apkārtmēru, nosakiet sirdsdarbības ātrumu un izmēra asinsspiedienu (BP) abās rokās. Visiem pacientiem jāveic perifērā pulsa palpācija, miega, subklāvijas un augšstilba artēriju auskultācija. Netipiskas stenokardijas gadījumā tiek veikta palpācija sāpju punkti parasternālais reģions un starpribu telpas.
Pacienta ar aizdomām par CAD pamata izmeklēšanā ietilpst standarta bioķīmiskie testi. Vissvarīgākais parametrs ir lipīdu spektrs. Ieteicams noteikt asins lipīdu profilu tukšā dūšā, tostarp kopējā holesterīna (TC), augsta blīvuma lipoproteīnu holesterīna (ABL-C), zema blīvuma lipoproteīnu holesterīna (ZBL-C) un triglicerīdu līmeni.
Dislipoproteinēmija, nelīdzsvarotība starp galveno lipīdu klašu attiecību plazmā, ir galvenais aterosklerozes riska faktors. Ar ļoti augstu holesterīna līmeni IHD attīstās pat jauniem cilvēkiem. Hipertrigliceridēmija ir arī nozīmīgs aterosklerozes komplikāciju prognozētājs.
Glikozes līmenis plazmā tukšā dūšā un glikētā hemoglobīna (HbAlc) līmenis jānosaka katram pacientam, kuram ir aizdomas par CAD. Ja abi rezultāti ir nepārliecinoši, ieteicams veikt perorālo glikozes tolerances testu (OGTT).
Ja ir klīniskas aizdomas par nestabilu CAD, jāmēra miokarda bojājuma bioķīmisko marķieru, piemēram, troponīna T vai troponīna I, līmenis, vēlams, izmantojot ļoti vai ultrajutīgas metodes. Tā kā troponīniem ir galvenā loma nestabilu pacientu identificēšanā, ir ieteicams tos izmērīt katram pacientam, kas hospitalizēts simptomātiskas stabilas CAD dēļ.
Neinvazīvas metodes Sirds anatomijas novērtējumi var noteikt obstruktīvas koronāro artēriju slimības iespējamību ar pieņemamu noteiktības pakāpi.
Visiem pacientiem, kuriem ir aizdomas par CAD, ir jāreģistrē 12 novadījumu EKG miera stāvoklī. Nekomplicētas hroniskas išēmiskas sirds slimības gadījumā ārpus fiziskās slodzes specifiskas miokarda išēmijas EKG pazīmes parasti nav. Vienīgā specifiskā koronāro artēriju slimības pazīme miera stāvoklī esošajā EKG ir liela fokusa rētas izmaiņas miokardā pēc MI.
Daudz svarīgāka ir EKG reģistrācija sāpīga lēkmes laikā krūtīs. Ja sāpju laikā EKG izmaiņas nav, sirds išēmiskās slimības iespējamība šādiem pacientiem ir zema, lai gan tas nav pilnībā izslēgts. Jebkuru EKG izmaiņu parādīšanās sāpīga uzbrukuma laikā vai tūlīt pēc tā ievērojami palielina koronāro artēriju slimības iespējamību. Išēmiskas EKG izmaiņas vairākos vados vienlaikus ir nelabvēlīga prognostiska zīme.
Stresa testi ir indicēti visiem pacientiem, kuriem ir aizdomas par slodzes stenokardiju un kuriem ir liela koronāro artēriju slimības iespējamība (15-85%). Indikācijas stresa testēšanai personām ar iepriekš noteiktu koronāro artēriju slimības diagnozi: sākotnējā un atkārtotā komplikāciju riska stratifikācija, medikamentozās un ķirurģiskās ārstēšanas efektivitātes novērtējums.
Parasti tiek veikts veloergometra tests (VEM tests) vai skrejceļa tests. Staigāšanas tests (tests skrejceļā) ir vairāk fizioloģisks, un to biežāk izmanto, lai noteiktu koronāro artēriju slimību pacientu funkcionālo klasi. Veloergometrija ir informatīvāka sirds išēmiskās slimības noteikšanā neskaidros gadījumos, taču tai ir nepieciešamas vismaz elementāras riteņbraukšanas prasmes, grūtāk veikt gados vecākiem pacientiem un ar vienlaicīgu aptaukošanos.
Priekškambaru transezofageālās stimulācijas (TEES) izplatība koronāro artēriju slimības ikdienas diagnostikā ir mazāka, lai gan šī metode informācijas satura ziņā ir salīdzināma ar VEM testu un skrejceļa testu. TEES metode ir izvēles līdzeklis gadījumos, kad pacients nevar veikt citus slodzes testus nekardiālu faktoru dēļ (muskuļu un skeleta sistēmas slimības, intermitējoša klusums, tendence uz izteiktu asinsspiediena paaugstināšanos dinamiskas fiziskās slodzes laikā, attrenēšanās, elpošanas mazspēja).
Farmakoloģisko testu veikšanas metode ir balstīta uz miokarda išēmijas lēkmes provocēšanu, izmantojot zāles ar vienlaicīgu EKG ierakstīšanu. Atkarībā no ievadītā medikamenta tiek veikti testi ar vazodilatatoru (dipiridamolu) vai ar inotropisku līdzekli (dobutamīnu). Šīs zāles tiek ievadītas intravenozi intensīvās terapijas nodaļā, stingri kontrolējot asinsspiedienu un sirdsdarbības ātrumu, nepārtraukti kontrolējot EKG.
Ambulatorā (Holtera) EKG monitorēšana ir indicēta visiem pacientiem ar koronāro artēriju slimību, ja ir aizdomas par vienlaicīgām aritmijām, kā arī ja nav iespējams veikt slodzes testu blakusslimību dēļ (muskuļu un skeleta sistēmas slimības, intermitējoša kludikācija, tendence uz izteiktu pieaugumu asinsspiedienā dinamiskas fiziskās slodzes laikā, atslābināšanās, elpošanas mazspēja). Ļauj noteikt sāpīgas un klusas miokarda išēmijas sastopamību, kā arī veikt diferenciāldiagnozi ar vazospastisku stenokardiju.
Ultrasonogrāfija miega artērijas veic pacientiem, kuriem diagnosticēta koronāro artēriju slimība un mērens risks smagas komplikācijas lai novērtētu aterosklerozes smagumu un izplatību. Turklāt visiem pacientiem ar koronāro artēriju slimību, kam paredzēta ķirurģiska miokarda revaskularizācija, tiek veikta miega artēriju ultraskaņa.
Ehokardiogrāfisko izmeklēšanu (sirds ultraskaņu) miera stāvoklī veic visiem pacientiem ar aizdomām un pierādītu hroniskas išēmiskas sirds slimības diagnozi. Ehokardiogrāfijas (EchoCG) galvenais mērķis miera stāvoklī ir stenokardijas diferenciāldiagnoze ar nekoronārām sāpēm krūtīs, ko izraisa aortas vārstuļa defekti, perikardīts, augšupejošās aortas aneirismas, hipertrofiska kardiomiopātija, mitrālā vārstuļa prolapss un citas slimības.
Stresa ehokardiogrāfija ir viena no populārākajām un ļoti informatīvākajām metodēm koronāro artēriju slimības neinvazīvai diagnostikai. Metodes pamatā ir kreisā kambara lokālas disfunkcijas vizuāla noteikšana fiziskas slodzes laikā (uz skrejceliņa vai veloergometra) vai farmakoloģiskā pārbaude. Stresa ehokardiogrāfija ir pārāka par parasto stresa EKG diagnostiskajā vērtībā, tai ir lielāka jutība (80-85%) un specifiskums (84-86%) koronāro artēriju slimības diagnostikā. Ja tehniski iespējams, metode ir indicēta visiem pacientiem ar pierādītu koronāro artēriju slimību, lai pārbaudītu ar simptomiem saistīto koronāro artēriju, kā arī gadījumā, ja sākotnējās diagnostikas laikā tiek iegūti apšaubāmi parastā stresa testa rezultāti.
Visiem pacientiem ar koronāro artēriju slimību tiek veikta krūškurvja orgānu rentgena izmeklēšana. Tomēr šis pētījums ir visvērtīgākais personām ar pēcinfarkta kardiosklerozi, sirds defektiem, perikardītiem un citiem vienlaicīgas sirds mazspējas cēloņiem, kā arī gadījumos, kad ir aizdomas par augšupejošās aortas arkas aneirismu.
Sirds magnētiskās rezonanses attēlveidošanu (MRI) miera stāvoklī var izmantot arī, lai noteiktu sirds strukturālās novirzes un novērtētu sirds kambaru funkciju. Sirds MRI ir ieteicama pacientiem, kuriem, neskatoties uz atbalss kontrastvielu lietošanu, transtorakālā ehokardiogrāfija nesniedz atbildi uz klīnisko jautājumu (parasti nepietiekama akustiskā loga dēļ), ja vien nav kontrindikāciju sirds MRI veikšanai.
Sirds MRI ar farmakoloģisku iedarbību ar dobutamīna infūziju var izmantot, lai identificētu išēmijas izraisītas sienas kustības anomālijas. Ir pierādīts, ka šai metodei ir līdzīgas drošības īpašības kā dobutamīna stresa ehokardiogrāfijai.
Radioizotopu izpētes metodes ietver miokarda perfūzijas scintigrāfiju (vienfotona emisijas datortomogrāfija un pozitronu emisijas tomogrāfija), jutīgu un ļoti specifisku pētījumu metodi ar augstu prognostisko nozīmi. Radiofarmaceitiskie preparāti tehnēcijs-99t (99mTc) ir visplašāk izmantotie marķieri, ko izmanto viena fotona emisijas datortomogrāfijā (SPECT).
Scintigrāfijas kombinācija ar fiziskām aktivitātēm vai farmakoloģiskajiem testiem (dobutamīna, dipiridamola intravenoza ievadīšana dozētā veidā) ievērojami palielina iegūto rezultātu vērtību. Būtisku asins piegādes traucējumu konstatēšana scintigrāfisko pētījumu laikā pacientiem ar koronāro artēriju slimību norāda uz nelabvēlīgu prognozi un kalpo par pārliecinošu pamatu koronārās angiogrāfijas veikšanai ar sekojošu lēmumu par miokarda ķirurģiskas revaskularizācijas jautājumu.
Neinvazīvās koronāro artēriju anatomijas novērtēšanas metodes sastāv no koronārā kalcija indeksa noteikšanas, koronāro artēriju magnētiskās rezonanses attēlveidošanas un koronāro artēriju elektronstaru tomogrāfijas.
Mūsdienu multidetektoru (vairāku slāņu) CT sistēmu telpiskā un laika izšķirtspēja un apjoma pārklājums ir pietiekams, lai daudziem pacientiem iegūtu skaidrus koronāro artēriju attēlus. Viena no problēmām ir radiācijas deva, un, izmantojot datortomogrāfiju (CT), lai attēlotu koronāro artēriju, īpaši jāuzmanās, lai izvairītos no nevajadzīgi lielām starojuma devām. Koronāro artēriju CT attēlveidošanu var veikt bez kontrastvielas ievadīšanas (lai noteiktu koronārā kalcija indeksu) vai pēc jodu saturoša kontrasta (koronāro artēriju CTA) intravenozas injekcijas.
Koronārā kalcija indekss. Daudzdetektoru CT var noteikt koronāro artēriju pārkaļķošanos datu kopās bez kontrasta. Pēc vienošanās par koronāro kalciju uzskata pikseļus, kuru blīvums pārsniedz sliekšņa vērtību 130 Haunsfīldas vienības (HU). Kalcificētos bojājumus parasti kvantitatīvi nosaka, izmantojot Agatston indeksu.
Koronārās magnētiskās rezonanses angiogrāfija (MRA) nodrošina koronāro artēriju neinvazīvu vizualizāciju, ja pacients netiek pakļauts jonizējošajam starojumam. Priekšrocības šī metode iekļaut sirds anatomijas un funkcijas globālu novērtējumu vienā pētījumā. Tomēr šobrīd koronārā MRA joprojām ir jāuzskata par pētniecības instrumentu, un tā nav ieteicama ikdienas klīniskajā praksē CAD diagnostiskajā novērtēšanā.
Koronāro artēriju elektronstaru tomogrāfiju izmanto koronāro artēriju aterosklerozes diagnostikā, īpaši daudzu asinsvadu bojājumu un kreisās galvenās koronārās artērijas bojājumu pārbaudē. Tomēr plašai lietošanai šī metode joprojām ir nepieejama, dārga un tai ir vairāki ierobežojumi. Šī pētījuma vispārēja veikšanas iespējamība sirds išēmiskās slimības gadījumā vēl nav pierādīta.
Neinvazīvo diagnostikas pētījumu galvenais mērķis ir iedalīt pacientus ar pierādītu CAD grupās ar augstu, vidēju vai zemu smagu komplikāciju un letālu iznākumu risku.
Ceļā uz invazīvām metodēm sirds artēriju pētīšanai ietver koronāro artēriju CT angiogrāfiju, koronāro angiogrāfiju, koronāro artēriju multispirālo rentgena datortomogrāfiju, intrakoronāro ultrasonogrāfija.
Koronāro artēriju CT angiogrāfija (CTA). Pēc intravenozas injekcijas kontrastviela CT ļauj vizualizēt koronāro artēriju lūmenu. Būtiska ir adekvāta tehnoloģiju (vismaz 64 slāņu CT) un pacientu atlase, kā arī rūpīga pacienta sagatavošana. Pēc ekspertu domām, koronārā CTA jāapsver tikai pacientiem ar adekvātu elpas aizturēšanas spēju, bez smagas aptaukošanās un ar labvēlīgu kalcija indeksu.
Koronārā angiogrāfija (CAG) ir “zelta standarts”, lai identificētu un novērtētu koronāro artēriju slimību. Indikācijas CAG hroniskas išēmiskas sirds slimības gadījumā: sirds išēmiskās slimības diagnozes pārbaude neskaidros gadījumos; miokarda revaskularizācijas taktikas noteikšana pierādītai koronāro artēriju slimībai: neefektivitātes gadījumā narkotiku ārstēšana IHD; ar augstu kardiovaskulāro komplikāciju risku saskaņā ar klīniskajiem datiem un neinvazīvo pētījumu rezultātiem.
Dažreiz koronāro angiogrāfiju papildina ar ventrikulogrāfisko izmeklēšanu. Galvenā ventrikulogrāfijas indikācija ir detalizēts vispārējās un lokālās kreisā kambara kontraktilitātes novērtējums. Ar ventrikulogrāfiju konstatētā kreisā kambara disfunkcijas vērtība ir ļoti svarīga, lai prognozētu visu veidu koronāro artēriju slimību pacientu izdzīvošanu. Ventrikulogrāfija tiek veikta, ja ehokardiogrāfiskā izmeklēšana ir neinformatīva.
Koronāro artēriju daudzslāņu rentgena datortomogrāfija ir alternatīva tradicionālajai invazīvai koronārajai angiogrāfijai koronāro artēriju slimības diagnostikā neskaidros gadījumos, un to var veikt uz tām pašām indikācijām. Pēc intravenoza ievadīšana Rentgena kontrastviela var vizualizēt koronārās artērijas un šuntus uz tām, diezgan precīzi noteikt aterosklerozes plāksnes un noteikt intravaskulārās stenozes pakāpi. Metodes priekšrocība ir tās minimālā invazivitāte. Gados vecākiem pacientiem ar vairākām pārkaļķotām intravaskulārām plāksnēm šī metode bieži noved pie koronāro artēriju stenozes pārmērīgas diagnostikas. Pierādītas koronāro artēriju slimības un ķirurģiskas revaskularizācijas metodes izvēles gadījumā vēlams veikt CAG.
Intrakoronārā ultraskaņa (IC-US) ir salīdzinoši jauna metode diagnostikas pētījums, kas papildina koronāro angiogrāfiju. Tas ir brīvs no dažiem CAG trūkumiem, jo tas ļauj izpētīt aterosklerozes plankumu virsmu un iekšējo struktūru, identificēt koronāro artēriju trombozi un pārbaudīt asinsvadu sieniņas stāvokli ap plāksnēm. Turklāt ar Vc-ultraskaņas palīdzību ir iespējams precīzāk pārbaudīt sarežģītas konfigurācijas plāksnes, kuras ir grūti kvantitatīvi noteikt ar koronāro angiogrāfiju parastajās projekcijās.
Koronārā sirds slimība (KSS) ir akūts vai hronisks sirds bojājums, ko izraisa miokarda asins piegādes samazināšanās vai pārtraukšana koronāro artēriju aterosklerozes procesa dēļ, kā rezultātā rodas neatbilstība starp koronāro asins plūsmu un miokarda skābekļa patēriņu. IHD ir visvairāk kopīgs iemesls priekšlaicīga nāve un invaliditāte visās rūpnieciski attīstītajās pasaules valstīs. Mirstība no IHD Ukrainā ir 48,9% no kopējās mirstības (2000:) ASV puse no visām pusmūža cilvēku slimībām ir IHD, un tās izplatība ar katru gadu pieaug. Daudzu epidemioloģisko pētījumu dati ir ļāvuši formulēt koronāro artēriju slimības riska faktoru jēdzienu. Saskaņā ar šo koncepciju riska faktori ir ģenētiski, eksogēni, endogēni vai funkcionāli noteikti apstākļi vai īpašības, kas nosaka paaugstinātu koronāro artēriju slimības attīstības iespējamību personām, kurām tās nav.Tie ietver vīriešu dzimumu (vīrieši saslimst ar IHD agrāk un biežāk nekā sievietes); vecums (koronāro artēriju slimības attīstības risks palielinās līdz ar vecumu, īpaši pēc 40 gadiem); iedzimta predispozīcija (vecākiem ir IHD, hipertensija un to komplikācijas līdz 55 gadu vecumam); dislipoproteinēmija: hiperholesterinēmija (kopējā holesterīna līmenis tukšā dūšā virs 5,2 mmol/l), hipertrigliceridēmija (triglicerīdu līmenis asinīs 2,0 mmol/l vai vairāk), hipoalfaholesterinēmija (0,9 mmol/l vai mazāk); liekā ķermeņa masa; smēķēšana (regulāri izsmēķēt vismaz vienu cigareti dienā); fiziska neaktivitāte (zema fiziskā aktivitāte) - darbs sēžot vairāk nekā pusi no darba laika un neaktīvs brīvais laiks (pastaigas, sportošana, darbs dārzā u.c. mazāk par 10 stundām nedēļā); paaugstināts psihoemocionālā stresa līmenis (stresa-koronārais profils); cukura diabēts; hiperurēmija, hiperhomocisteinēmija. Pašlaik tiek uzskatīti par galvenajiem riska faktoriem notāra hipertensija, hiperholesterinēmija un smēķēšana (“lielais trijnieks”).
Etioloģija
Galvenie IHD etioloģiskie faktori ir: - Koronāro artēriju, galvenokārt to proksimālo daļu, ateroskleroze (95% pacientu ar IHD). Visbiežāk tiek skarts kreisās koronārās artērijas priekšējais interventrikulārais zars, retāk labā koronārā artērija, tad kreisās koronārās artērijas cirkumfleksais zars. Visbīstamākā aterosklerozes lokalizācija ir kreisās koronārās artērijas galvenais stumbrs; - Koronāro artēriju spazmas, kas lielākajai daļai pacientu ar koronāro artēriju slimību rodas uz aterosklerozes fona. Ateroskleroze izkropļo koronāro artēriju reaktivitāti, palielinot to jutību pret vides faktoriem. - Koronāro artēriju tromboze, kā likums, to aterosklerozes bojājuma klātbūtnē. Reti miokarda išēmija rodas koronāro artēriju iedzimtu anomāliju, to embolijas, koronāro artēriju slimības un koronāro artēriju sašaurināšanās ar sifilītu smaganu rezultātā. Uz attīstību provocējošiem faktoriem klīniskās izpausmes IHD ietver fiziskās aktivitātes, stresa emocionālas un psihosociālas situācijas. Daļēji aterosklerozi kompensējošs faktors ir blakus cirkulācija.Patoģenēze
Galvenais IHD patofizioloģiskais mehānisms ir neatbilstība starp miokarda pieprasījumu pēc skābekļa un koronārās asinsrites spēju apmierināt šīs vajadzības. Galvenie šīs neatbilstības iemesli ir: 1. Samazināta koronārā asins plūsma koronāro artēriju bojājumu dēļ. 2. Sirds darba stiprināšana, palielinoties tās vielmaiņas vajadzībām. 3. Asinsvadu un vielmaiņas faktoru kombinācija. Miokarda skābekļa patēriņu nosaka sirdsdarbības ātrums; miokarda kontraktilitāte - pēc sirds izmēra un asinsspiediena vērtības. IN normāli apstākļi ir pietiekama koronāro artēriju (KA) dilatācijas rezerve, nodrošinot iespēju pieckārtīgi palielināt koronāro asins plūsmu un līdz ar to arī skābekļa piegādi miokardam. Neatbilstība starp miokarda vajadzību pēc skābekļa un tā piegādi var rasties smagas koronāro artēriju aterosklerozes, to spazmas un koronāro artēriju aterosklerozes bojājumu un vazospazmu kombinācijas rezultātā, t.i. to organiskā un dinamiskā obstrukcija. Organiskās obstrukcijas cēlonis ir koronāro artēriju ateroskleroze. Krasais koronārās asinsrites ierobežojums šajos gadījumos skaidrojams ar aterogēno lipoproteīnu sieniņu infiltrāciju, fibrozes attīstību, aterosklerozes plāksnes veidošanos un artērijas stenozi. Noteikta nozīme ir arī asins recekļa veidošanās koronārajā artērijā. Dinamisku koronāro obstrukciju raksturo koronāro spazmu attīstība uz aterosklerozes izmaiņu fona koronārajās artērijās. Saskaņā ar “dinamiskās stenozes” jēdzienu koronārās artērijas lūmena sašaurināšanās pakāpe ir atkarīga gan no organiskā bojājuma pakāpes, gan no spazmas smaguma pakāpes. Spazmas ietekmē kuģa sašaurinātais lūmenis var palielināties līdz kritiskajam līmenim (75%), kas izraisa stenokardijas attīstību. Koronārās spazmas attīstībā ir iesaistīta simpātiskā nervu sistēma un tās mediatori, peptīdi, piemēram, viela P un neirotenzīns, arahidonskābes metabolīti - prostaglandīns F2a, leikotriēni. Vietējiem vielmaiņas faktoriem ir liela nozīme koronārās asinsrites regulēšanā. Samazinoties koronārajai asins plūsmai, miokarda vielmaiņa pāriet uz anaerobo ceļu un tajā uzkrājas metabolīti, kas paplašina koronārās artērijas (adenozīns, pienskābe, inozīns, hipoksantīns). Koronāro artēriju slimības gadījumā aterosklerozes procesa izmainītās koronārās artērijas nevar adekvāti paplašināties atbilstoši palielinātajai miokarda skābekļa nepieciešamībai, kas izraisa išēmijas attīstību. Endotēlija faktori ir būtiski. Endotelīni 1, 2,3 tiek ražoti endotēlijā. Endotelīns 1 ir visspēcīgākais zināmais vazokonstriktors. Tās vazokonstriktora darbības mehānisms ir saistīts ar kalcija satura palielināšanos gludās muskulatūras šūnās. Endotēlijs arī stimulē trombocītu agregāciju. Turklāt endotēlijs ražo prokoagulējošas vielas: audu tromboplastīnu, fon Vilebranda faktoru, kolagēnu, trombocītu aktivējošo faktoru. Līdztekus vielām, kurām ir vazokonstriktora un prokoagulējoša iedarbība, endotēlijs rada arī faktorus, kuriem ir vazodilatatora un antikoagulanta iedarbība. Tie ietver prostatas ciklu un endotēlija relaksācijas faktoru (ERF). ERP apzīmē slāpekļa oksīdu (NO) un ir spēcīga azodilatējoša un prettrombocītu viela. Prostaciklīnu galvenokārt ražo endotēlijs un mazākā mērā gludās muskulatūras šūnas. Tam ir izteikta koronāro asinsvadu paplašināšanas iedarbība, kavē trombocītu agregāciju, ierobežo miokarda infarkta zonu. agrīnā stadijā, uzlabo enerģijas apmaiņu išēmiskajā miokardā un novērš laktāta un piruvāta uzkrāšanos tajā; piemīt antiaterosklerozes iedarbība, samazinot lipīdu uzņemšanu asinsvadu sieniņās. Koronāro artēriju aterosklerozes gadījumā endotēlija spēja sintezēt prostaciklīnu ir ievērojami samazināta. IHD gadījumā palielinās trombocītu agregācija un mikroagregātu parādīšanās koronāro artēriju mazajos zaros, kas izraisa mikrocirkulācijas traucējumus un miokarda išēmijas saasināšanos. Paaugstināta trombocītu agregācija ir saistīta ar palielinātu trombocītu un tromboksāna veidošanos. Parasti pastāv dinamisks līdzsvars starp tromboksānu (propacītu līdzekli un vazokonstriktoru) un prostaciklīnu (prettrombocītu līdzekli un vazodilatatoru). Ar išēmisku sirds slimību šis līdzsvars tiek traucēts un palielinās tromboksāna aktivitāte. Pacientiem ar koronāro artēriju slimību ar stenozējošu koronāro aterosklerozi un attīstītām blakusparādībām slodzes laikā vazodilatācijas rezultātā palielinās asins plūsma koronārajās artērijās, kuras nav skārusi ateroskleroze, ko pavada asins plūsmas samazināšanās slimajā. artērija distālā no stenozes, “starpkoronārās zagšanas” fenomena attīstība un miokarda išēmija. Nodrošinājumu attīstība daļēji kompensē koronārās asinsrites traucējumus pacientiem ar koronāro artēriju slimību. Tomēr ar izteiktu miokarda skābekļa pieprasījuma pieaugumu, nodrošinājumi nekompensē asins piegādes deficītu. IHD gadījumā palielinās lipīdu peroksidācijas (LPO) aktivitāte, kas aktivizē trombocītu agregāciju. Turklāt lipīdu peroksidācijas produkti pastiprina miokarda išēmiju. Endogēno opioīdu peptīdu (nekefalīnu un endorfīnu) ražošanas samazināšanās veicina miokarda išēmijas attīstību un progresēšanu.Klīnika
Koronāro artēriju slimības klīniskā klasifikācija (2002) Pēkšņa koronārā nāve Pēkšņa klīniska koronārā nāve ar veiksmīgu reanimāciju. Pēkšņa koronārā nāve (letāls iznākums). Stenokardija Stabila stenokardija (norāda funkcionālās klases) Stabila stenokardija ar angiogrāfiski neskartiem asinsvadiem (koronārais sindroms X) Vazospastiska stenokardija (spontāna, variants, Princmetāls) Nestabila stenokardija Jauni sastopama stenokardija Progresējoša stenokardija Agrīna pēcinfarkta stenokardija (no 28 dienām) pēc miokarda infarkta).Akūts miokarda infarkts Akūts miokarda infarkts ar patoloģisku Q viļņu (transmurāls, liels fokuss) Akūts miokarda infarkts bez patoloģiska Q viļņa (mazs fokuss) Akūts subendokarda miokarda infarkts Akūts miokarda infarkts (neprecizēts) I Atkārtots (neprecizēts) I recidīvs 2 8 dienas) Atkārtots miokarda infarkts (pēc 28 dienām) Akūta koronārā mazspēja (ST segmenta pacēlums vai depresija) Kardioskleroze Fokālā kardioskleroze Pēcinfarkta kardioskleroze, kas norāda uz sirds mazspējas formu un stadiju, ritma raksturu un vadīšanas traucējumiem, skaitu infarktu, to atrašanās vieta un rašanās laiks, Hroniska sirds aneirisma Fokālā kardioskleroze, bez indikācijas par iepriekšēju miokarda infarktu Difūza kardioskleroze, kas norāda uz sirds mazspējas formu un stadiju, ritma un vadīšanas traucējumiem Klusā koronāro artēriju slimības forma Diagnozes pamatā ir miokarda konstatēšana išēmija, izmantojot slodzes testu, Holtera monitorēšanas EKG ar verifikāciju saskaņā ar koronāro angiogrāfiju, miokarda scintigrāfiju ar talliju, stresa ehokardiogrāfiju stenokardijas UN MIOKARDA INFRAKTA APRAKSTU SKAT. ATTIECĪGĀS IEDAĻAS PĒKŠŅA KORONĀRĀ NĀVE (PRIMĀRĀ SIRDS JOPROJĀM) Pēkšņa koronārā nāve ir nāve liecinieku klātbūtnē, kas iestājas nekavējoties vai 6 stundu laikā pēc sirdslēkmes sākuma, iespējams, saistīta ar miokarda elektrisko nestabilitāti, ja nav pazīmju, ļauj veikt citu diagnozi.
Pēkšņu koronāro nāvi visbiežāk izraisa kambaru fibrilācija. Provocējošie faktori ir fiziskais un psihoemocionālais stress, alkohola lietošana, kas izraisa miokarda skābekļa pieprasījuma palielināšanos.
Pēkšņas koronārās nāves riska faktori ir krasa slodzes tolerances samazināšanās, ST segmenta nomākums, ventrikulāras ekstrasistoles (īpaši biežas vai politopiskas) slodzes laikā un iepriekš pārciests miokarda infarkts. Klīnika: pēkšņas nāves kritēriji ir samaņas zudums, elpošanas apstāšanās vai pēkšņa atonāla elpošana, pulsa trūkums lielajās artērijās (miega un augšstilba kaula), sirds skaņu trūkums, paplašinātas acu zīlītes un gaiši pelēkas ādas izskats. tonis.
EKG ir redzamas liela vai maza viļņa ventrikulāras fibrilācijas pazīmes: kambaru kompleksa raksturīgo kontūru izzušana, dažāda augstuma un platuma neregulāru viļņu parādīšanās ar frekvenci 200-500 minūtē. Var būt sirds asistolija, ko raksturo trūkums EKG viļņi, vai sirds elektromehāniskās disociācijas pazīmes (rets sinusa ritms, kas var pārvērsties par idioventrikulāru, kam seko asistolija).
Laika intervāls starp trešo un ceturto izlādi nedrīkst pārsniegt 2 minūtes. Adrenalīna ievadīšana jāatkārto aptuveni ik pēc 2-3 minūtēm.
Pēc trim defibrilācijas cikliem ar 360 J izlādi tiek veikta nātrija bikarbonāta intravenoza pilināšana, tiek veikti pasākumi, lai novērstu smadzeņu hipoksijas attīstību: tiek nozīmēti antihipoksanti (nātrija hidroksibutirāts, seduksēns, piracetāms), līdzekļi, kas samazina nātrija bikarbonāta caurlaidību. asins-smadzeņu barjera (glikokortikosteroīdi, proteāzes inhibitori, askorbīnskābe); tiek lemts jautājums par antiaritmisko līdzekļu (b-blokatoru vai amnodarona) lietošanu. Asistolijas gadījumā tiek veikta transvenoza endokarda vai perkutāna sirds stimulēšana.
Reanimācijas pasākumi tiek pārtraukti, ja tiek ievēroti šādi kritēriji: ilgstošas atdzīvināšanas laikā (vismaz 30 minūtes) nav sirdsdarbības atjaunošanās pazīmju; smadzeņu nāves pazīmes (nav spontānas elpošanas, skolēni nereaģē uz gaismu, nav smadzeņu elektriskās aktivitātes pazīmju pēc elektroencefalogrāfijas), hroniskas slimības beigu periods. Pēkšņas nāves profilakse sastāv no koronāro artēriju slimības progresēšanas novēršanas, miokarda elektriskās nestabilitātes savlaicīgas noteikšanas un sirds ritma kambaru traucējumu novēršanas vai novēršanas.
BEZSĀPES MIOKARDIĀLĀ IZĒMIJA Klusās miokarda išēmijas (SMI) diagnoze balstās uz miokarda išēmijas pazīmju identificēšanu elektrokardiogrammā, izmantojot slodzes testu (veloergometriju, skrejceliņu), un to pārbauda ar koronāro angiogrāfiju, tallija miokarda scintigrāfiju un stresa ehokardiogrāfiju. Visticamāko informāciju par ĶMI klātbūtni pacientam, tā smagumu, ilgumu, apstākļiem un rašanās laiku dienas laikā var iegūt, izmantojot Holtera monitoringa (HM) EKG metodi.
Novērtējot ikdienas išēmisko aktivitāti un jo īpaši kluso miokarda išēmiju, vissvarīgākā kļūst ST segmenta išēmiskā nobīdes pareiza noteikšana. Saskaņā ar mūsdienu kritērijiem tiek ņemta vērā ST segmenta depresija ar amplitūdu vismaz 1 mm, ilgums ir vismaz 1 minūte, ar laika intervālu starp divām epizodēm vismaz 1 minūti (“trīs vienību” noteikums).
Šajā gadījumā tiek ņemta vērā tikai horizontālā vai slīpā nobīde uz leju vismaz 0,08 s no punkta j.Pēc HM datiem tiek noteikti šādi nozīmīgākie rādītāji: išēmisku epizožu skaits diennakts laikā; ST segmenta depresijas vidējā amplitūda (mm); išēmiskās epizodes vidējais sirdsdarbības ātrums (saīsinājumi/min); vienas išēmiskās epizodes vidējais ilgums (min); kopējais išēmijas ilgums dienā (min).
Šo rādītāju salīdzinošā analīze tiek veikta arī dienas un nakts periodiem, kā arī sāpīgai un nesāpīgai miokarda išēmijai. Palielinoties asinsvadu gultnes bojājuma pakāpei un pastiprinoties klīniskajiem simptomiem, palielinās klusās miokarda išēmijas biežums.
Sāpīgo un “kluso” ST segmenta pārvietošanās epizožu skaits dienā saskaņā ar Holtera EKG monitoringu izrādījās maksimālais pacientiem ar daudzu asinsvadu koronāro artēriju slimību un pacientiem ar progresējošu stenokardiju. Kopējais nesāpīgās miokarda išēmijas ilgums ir atkarīgs arī no aterosklerotisko izmaiņu izplatības un smaguma koronārajās artērijās.
“Klusā” miokarda išēmija, kas ilgst vairāk nekā 60 minūtes/24 stundas, ir īpaši izplatīta, ja procesā tiek iesaistīti visi trīs koronāro artēriju atzari un tiek ietekmēts kreisās koronārās artērijas galvenais stumbrs pacientiem ar stabilu stenokardiju. augstas funkcionālās klases un nestabila (progresējoša) stenokardija. Kopā ar Holtera EKG uzraudzību ehokardiogrāfija ir būtiska, lai identificētu "kluso" išēmiju.
Koronārās sirds slimības ehokardiogrāfijas diagnostikas iespējas slēpjas vairāku tās izpausmju un komplikāciju identificēšanā: 1. Vietējās miokarda asinerģijas zonas, kas atbilst stenozējošās koronārās artērijas asins piegādei.
2. Kompensējošās hiperfunkcijas zonas (hiperkinēzija, hipertrofija), atspoguļojot miokarda funkcionālo rezervi.
3. Iespējas neinvazīvi noteikt vairākus svarīgus sirds saraušanās un sūknēšanas funkcijas neatņemamos rādītājus - izsviedes frakciju, insultu un sirds indeksus, vidējo apļveida šķiedru saīsināšanas ātrumu u.c.
4. Aterosklerozes procesa bojājumu pazīmes aortai un tās galvenajām zarām, ieskaitot labās un kreisās koronāro artēriju stumbrus (sienu sabiezējums, mobilitātes samazināšanās, lūmena sašaurināšanās).
5. Akūtas un hroniskas aneirismas, papilāru muskuļu disfunkcija miokarda infarkta dēļ.
6. Difūzā kardioskleroze ar sirds kreisās un labās daļas paplašināšanos, tās kopējās sūknēšanas funkcijas krasu samazināšanos.
Šīs metodes izmantošana dažādos funkcionālos un farmakoloģiskajos testos būtiski palielina EchoCG informācijas saturu koronāro artēriju slimības agrīnā diagnostikā, īpaši tās nesāpīgajā norisē. Miokarda išēmijas marķieri stresa testu laikā ir vietējās kontraktilitātes traucējumi (asinerģija), traucēta diastoliskā funkcija, izmaiņas elektrokardiogrammā un stenokardijas sindroms.
Ehokardiogrāfijas iespējas farmakoloģisko testu laikā (dipiridamols, dobutamīns) ir identificēt slēptu miokarda išēmiju (asinerģiju), noteikt dzīvotspējīgu miokardu traucētas asins piegādes zonā, novērtēt kopējo sūknēšanas funkciju, miokarda kontraktilās rezerves un novērtēt koronāro artēriju slimības prognoze.
Ārstēšana
Neatliekamā palīdzība PĒKŠŅAS KORONĀRĀS NĀVES gadījumā. Sirds aktivitātes un elpošanas atjaunošana tiek veikta 3 posmos: 1. posms - caurlaidības atjaunošana elpceļi: pacients tiek noguldīts horizontāli uz muguras, uz cietas virsmas, galva tiek atmesta atpakaļ, ja nepieciešams, apakšžoklis tiek stumts uz priekšu un pēc iespējas uz augšu, satverot to ar abām rokām. Tā rezultātā mēles saknei vajadzētu attālināties no rīkles aizmugurējās sienas, nodrošinot brīvu gaisa piekļuvi plaušām.2. posms - mākslīgā ventilācija: aizveriet nāsis ar pirkstiem, elpojiet no mutes mutē ar frekvenci 12 minūtē. Varat izmantot elpošanas aparātu: Ambu maisu vai gofrētu plēšu RPA-1 tipa.
3. posms - sirdsdarbības atjaunošana, kas tiek veikta paralēli mehāniskajai ventilācijai. Tas, pirmkārt, ir ass sitiens ar dūri pa krūšu kaula lejasdaļu 1-2 reizes, slēgta sirds masāža, kas tiek veikta saskaņā ar šādiem noteikumiem: 1.
Pacients atrodas horizontālā stāvoklī uz cieta pamata (grīdas, dīvāna). 2.
Reanimatologa rokas atrodas krūšu kaula apakšējā trešdaļā stingri gar ķermeņa viduslīniju. 3.
Viena plauksta ir novietota uz otras; Rokas, kas iztaisnotas elkoņa locītavās, ir novietotas tā, lai spiedienu radītu tikai plaukstas. 4.
Krūšu kaula nobīdei pret mugurkaulu jābūt 4-5 cm, masāžas ātrumam jābūt 60 kustībām minūtē. Ja reanimāciju veic viens cilvēks, pēc divām gaisa injekcijām plaušās tiek veiktas 10-12 krūškurvja kompresijas (2:12).
Ja reanimācijā ir iesaistīti divi cilvēki, krūškurvja saspiešanas un mākslīgās elpināšanas attiecībai jābūt 5:1 (ik pēc 5 spiedieniem uz krūtis pauze 1-1,5 s ventilācijai). Plkst mākslīgā elpošana masāža tiek veikta caur endotraheālo cauruli bez pauzēm; ventilācijas biežums 12-15 minūtē.
Pēc sirds masāžas sākuma intravenozi vai intrakardiāli nekavējoties ievada 0,5-1 ml adrenalīna. Atkārtota ievadīšana iespējama pēc 2-5 minūtēm.
Efektīvāk ir ievadīt 1-2 ml Shadrin intravenozi vai intrakardiāli, pēc tam intravenozi pa pilienam. Efektu pastiprina, paralēli ievadot atropīna 0,1% šķīdumu 1-2 ml intravenozi.
Tūlīt pēc adrenalīna un atropīna infūzijas ievada nātrija bikarbonātu (200-300 ml 4% šķīduma) un prednizolonu - 3-4 ml 1% šķīduma. Ja ir defibrilators, sirds ritma atjaunošanai tiek izmantota defibrilācija, kas ir visefektīvākā lielu viļņu mirgošanas gadījumā.
Mazviļņu kambaru fibrilācijas gadījumā, kā arī neefektīvas defibrilācijas gadījumā intrakardiāli (1 cm līdz pa kreisi no krūšu kaula piektajā starpribu telpā). Veicot defibrilāciju, elektrodus var novietot divos veidos: 1.-II-III starpribu telpa krūšu kaula labajā pusē un sirds virsotnes laukums; 2.- zem lāpstiņas pa kreisi un IV starpribu telpa pa kreisi no krūšu kaula vai virs krūšu kaula.
Kardiopulmonālās reanimācijas shēma defibrilatora klātbūtnē Puncis sirds apvidū Defibrilācija ar izlādi 200 J Defibrilācija ar izlādi 200 - 300 J Defibrilācija ar izlādi 360 J Pacienta intubācija, nodrošinot savienojumu ar vēnu Adrenalīns 1 mg intravenozi Atkārtot kardiopulmonālās reanimācijas ciklu 10 reizes (5 kompresijas/1 injekcija) Defibrilācija ar izlādi 360 J Defibrilācija ar izlādi 360 J Defibrilācija ar izlādi 360 J. SĀPĪGAS MIOKARDA IZĒMIJAS ārstēšanai ir trīs galvenie mērķi:1) miokarda infarkta profilakse, 2) sirds funkcionālās slodzes samazināšana, 3) kvalitātes uzlabošana un paredzamā dzīves ilguma palielināšana.
Medikamentozā terapija ar antiangināliem līdzekļiem ietver nitrātu, kalcija antagonistu, (b-blokatoru lietošanu. Visas trīs antianginālo zāļu grupas ir efektīvas klusās miokarda išēmijas ārstēšanā, taču dati par to salīdzinošo efektivitāti ir neviennozīmīgi.
Tiek uzskatīts, ka beta blokatoriem ir vislielākā iedarbība pacientiem ar klusu išēmiju gan monoterapijā, gan kombinācijā ar ilgstošas darbības nitrozālēm. Tāpat kā ar koronāro artēriju slimības sāpīgajiem variantiem, “klusās” išēmijas ārstēšanā jāiekļauj lipīdu līmeni pazeminošas zāles un zāles, kuru mērķis ir normalizēt trombocītu funkcionālo stāvokli (spirīns, tiklids, plavikss).
Lai aktivizētu endogēno opioīdu sistēmu, kam piemīt kardioprotektīvas un vazodilatējošas īpašības, un nomāktu simpatoadrenālo sistēmu, ir attaisnojama pasākumu kompleksa izmantošana, kas ietver tādus nemedikamentozus līdzekļus kā refleksoloģija, kvantu hemoterapija un ultravioletā apstarošana. asinis. Ņemot vērā nelabvēlīgo klusās miokarda išēmijas prognozi, īpaši pacientiem ar stenokardiju un tiem, kam ir bijis miokarda infarkts, jāpieņem, ka savlaicīga ārstēšana palīdzēs palēnināt koronāro artēriju slimības progresēšanas ātrumu.
Uzmanību! Aprakstītā ārstēšana negarantē pozitīvs rezultāts. Lai iegūtu ticamāku informāciju, VIENMĒR konsultējieties ar speciālistu.